 B .
B .  C .
C .  D .
D . 




 B . 检查装置气密性
B . 检查装置气密性 C . 蒸发食盐水
C . 蒸发食盐水 D . 稀释浓硫酸
D . 稀释浓硫酸
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | N2 | O2 | 将气体缓缓通过足量的灼热铜网 |
B | CaO | CaCO3 | 加水溶解、过滤 |
C | NaOH | Na2CO3 | 加适量的Ca(OH)2溶液、过滤 |
D | FeCl2 | CuCl2 | 加入过量的铁粉,充分反应后过滤 |


①步骤一:关闭K2和K3 , 打开K1 , A中产生大量气泡。 为保证后续实验的成功,B中所盛放的溶液是。对比铁丝表面的变化,能够说明铁丝生锈与水有关的最佳装置是(填“C”、“D”或“E”,下同),能够说明铁丝生锈的快慢与氧气浓度有关的装置是。
②步骤二:关闭K1 , 打开K2和K3 , 将装置C、D中分液漏斗内的稀盐酸同时全部注入广口瓶中,C瓶中现象是;D瓶中溶液变成黄色反应的化学方程式为,由此也可以判断铁丝生锈情况。




①一氧化碳和二氧化碳化学性质不同的原因是;
②金刚石和石墨物理性质差异很大的原因是。

①A点表示的物质类别是。B点表示化合物的化学式为。
②某化合物化学式为(NH4)2Fe(SO4)2 , 它代表的点是。(填“A、B、C、D、E”)
③写出由C点表示的化合物与氧气、水发生化合反应生成D的化学方程式。

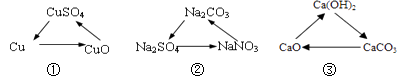
反应③的化学方程式为。
实验一:37%的浓盐酸(密度为1.19g/mL)、氢氧化钠溶液、蒸馏水、量筒、细口瓶等
①计算:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为mL(精确到0.1mL,下同);需要蒸馏水的体积为mL(水的密度为1.0g/mL)。
②量取:用量筒分别量取相应的浓盐酸和蒸馏水。
③。
④装瓶并贴上标签。

试计算该氢氧化钠溶液中溶质的质量分数。(在答题卡上写出计算过程)
猜想一:氧化钙;
猜想二:氢氧化钙;
猜想三:碳酸钙。
同学们经过分析将猜想一排除了,理由是。
(一)实验设计:
将一定量的乙炔(CxHy)在足量的氧气中完全燃烧,生成的气体全部缓缓通过下图装置(选填“Ⅰ”或“Ⅱ”)。

实验数据记录于下表中,试通过计算,确定乙炔的化学式。
反应前质量/g | 反应后质量/g | |
装置① | 125.3 | 127.1 |
装置② | 78.2 | 87.0 |
结论:乙炔的化学式。