 引燃酒精灯
B .
引燃酒精灯
B .  滴加试剂
C .
滴加试剂
C .  加热液体
D .
加热液体
D .  量取液体
量取液体
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别硬水和软水 | 取样加入肥皂水振荡 |
| B | 鉴别NH4NO3和NaOH固体 | 加水溶解观察溶液温度变化 |
| C | 鉴别羊毛和涤纶 | 取样点燃,闻燃烧产物的气味 |
| D | 比较Fe、Cu、Ag的金属活动性 | 将Fe分别加入Cu (NO3)2和AgNO3溶液中 |

①鸡蛋是生活中常见的食物,其富含的营养素是;
②青少年应均衡饮食,补充微量元素。若缺乏铁元素会引起。
城市居民小区内,应将生活垃圾按图示分三类科学处置。废旧干电池不能随意丢弃,应将其放入垃圾箱。

钙片的主要成分为碳酸钙,服用钙片后与胃酸反应的化学方程式为。
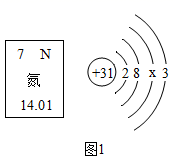
①氮元素是(填“金属元素”或“非金属元素”),氮原子的相对原子质量是;
②X=,氮化镓的化学式是。
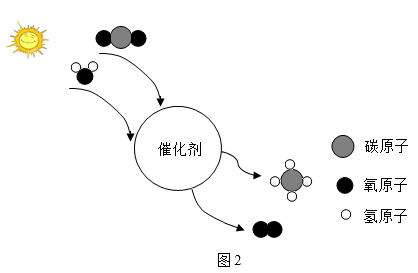
①该转化过程中,(填“原子”或“分子”)没有发生变化。
②该反应过程实现了将太阳能转化为。
③写出该过程的化学方程式:。

写出②中的反应方程式。若实验③中观察到了明显的现象。通过以上实验,判断三种金属的活动性由强到弱的顺序为。实验①~④中,不需要做的实验是(填序号)。

①a点对应的溶液是(填“饱和”或“不饱和”)溶液。
②a点对应的溶液的溶质质量分数是(只列计算式)。
③将a点对应的溶液升温到70 ℃,其溶质质量分数(填“变大”“变小”或“不变”)。
④欲使KNO3溶液的状态从b点转化为c点,可采取的措施是。


已知:白磷的着火点为40℃。
| 实验1 | 实验2 |
| I.将盛有足量锌粒的燃烧匙伸入瓶中,塞紧瓶塞 II.打开K,从长颈漏斗向瓶内加入稀盐酸,至浸没锌粒 III.当瓶中产生大量气泡时,关闭K | I.将盛有白磷的燃烧匙伸入瓶内,塞紧瓶塞 II.打开K,从长颈漏斗向瓶内加入约80℃的热水,至浸没白磷 III.从a口向瓶中鼓入空气,使瓶中液面低于燃烧匙底部,关闭K |
(问题提出)怎样证明NaOH溶液与稀盐酸能发生化学反应?

(查阅资料)可从三个方面设计实验证明:
一是设计实验证明反应物的消失;
二是设计实验证明有新物质生成;
三是设计实验证明化学反应有能量变化。
(实验探究)



a点表示溶液中的溶质是(写名称),将该溶液蒸发结晶后得到固体是 (填“纯净物”或“混合物”)
|
编号 |
盐酸 |
NaOH溶液 |
△t/℃ |
|
1 |
3.65% |
2.00% |
3.5 |
|
2 |
3.65% |
4.00% |
x |
|
3 |
7.30% |
8.00% |
14 |
表中x约为。