导弹是我国大国地位 、国防实力的显著标志。其制作材料中包含了 Fe 、Cr 、Ni 、C 等多种元素。回答下列问题:
①基态S原子核外有种不同空间运动状态的电子。
②已知H2S2O8的结构如图所示:
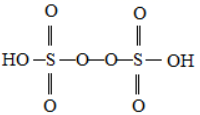
H2S2O8中硫原子的轨道杂化方式为;上述反应每生成1molMnO4— , S2O82—断裂的共价键类型及其数目分别为、(设阿伏加德罗常数的值为NA)
①请写出与CN—互为等电子体的一种分子:、一种离子:。
②组成尿素的第二周期元素的第一电离能由大到小的顺序为:,1molH2NCONH2(尿素)分子中含有σ键的数目为。
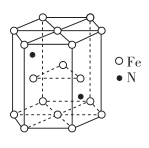
③FeN的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或b位置Fe,形成Cu替代型产物Fe(x—n)CunNy。
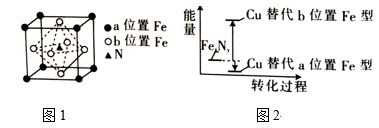
Cu处于周期表中区,其最高能层的符号为,基态铜原子的价电子排布式为。FexNy转化为两种Cu的替代型产物的能量变化如图2所示,其中相对不稳定的Cu替代型产物的化学式为。
①CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是(填“极性”或“非极性”)分子
②CrCl3·6H2O实际上是配合物,配位数是6,其固体有三种颜色,其中一种浅绿色固体于足量硝酸银反应时,1mol固体可生成1molAgCl沉淀,则这种浅绿色固体中阳离子的化学式为。