 洗涤试管
B .
洗涤试管
B .  熄灭酒精灯
C .
熄灭酒精灯
C .  称量NaOH固体
D .
称量NaOH固体
D .  取用块状固体
取用块状固体




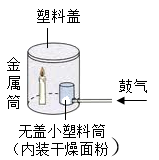 验证面粉具有可燃性
B .
验证面粉具有可燃性
B . 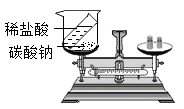 验证质量守恒定律
C .
验证质量守恒定律
C . 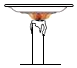 探究石蜡中含有碳元素
D .
探究石蜡中含有碳元素
D . 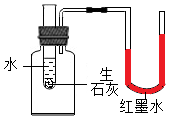 验证生石灰遇水放热,还可验证气体受热后分子间的间隔变大
验证生石灰遇水放热,还可验证气体受热后分子间的间隔变大
| 选项 | 实验目的 | 实验方案 |
| A | 检验二氧化碳 | 用燃着的木条伸入集气瓶内,观察火焰是否熄灭 |
| B | 实验室鉴别食盐和蔗糖 | 取样尝味道 |
| C | 除去盐酸溶液中的少量CuCl2 | 加入适量的NaOH溶液,过滤 |
| D | 除去KCl固体中少量的MnO2 | 加入足量的水溶解,过滤、蒸发结晶 |


①在101KPa时,氧气的溶解度曲线
②在装有空气的密闭容器中燃烧足量的红磷
③等质量、等质量分数的稀硫酸中分别加入足量的MgO和MgCO3 , 充分反应
④分别向质量为ag的镁粉和ag的铁粉中逐滴加入相同溶质质量分数的稀盐酸至过量

①氦元素。
②3个钠原子。
③1个臭氧分子。
④标出中五氧化二氮中氮元素的化合价。
①3Mg2+:。
②NH3。
|
物质 用途 |
|
干冰 用作建筑材料 小苏打 用于人工降雨 碳酸钙 用作焙制糕点的发酵粉 |
①不以化石能源为动力的是(填“煤”“柴油”或“纯电动”)公交车。
②从环境保护的角度考虑,下列燃料中最理想的是(填字母序号)。
A.酒精 B.汽油 C.氢气 D.天然气


①试管丙中观察到的现象是。
②M、Al、Cu三种金属的活动性由强到弱的顺序为。

①配制过程中有以下步骤:a.装瓶贴标签;b.计算;c.溶解:d.称量及量取。正确的顺序是(填字母序号)。
②将已配好的100g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量是g(计算结果精确到0.1)。


已知:I:H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ:CO2中混有的HCl气体可用饱和碳酸氢钠溶液吸收。
①装置甲中所盛的试剂应选用(填字母序号)。
A.NaOH溶液 B.浓硫酸 C.澄清石灰水 D.CuSO4溶液
②已知丙中所盛的试剂为浓硫酸,则丙装置的作用是。
③CO2气体的收集装置可以选用上图中的。(填“丁”或“戊”)
【提出问题】瓶口白色固体的成分是什么?
【查阅资料】①玻璃中含有二氧化硅(SiO2),试剂瓶身经过抛光处理,光滑且不易反应,而瓶口与玻璃塞接触处是磨砂玻璃,磨砂将二氧化硅裸棵露出来:
②二氧化硅能与氢氧化钠反应生成硅酸钠(Na2SiO3),Na2SiO3是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性:
③硅酸钠溶液能和强酸反应,如: ;
④Na2SiO3溶液和CaCl2溶液(呈中性)反应: 。
【作出猜想】白色固体的成分是:
猜想一:硅酸钠
猜想二:硅酸钠和碳酸钠
猜想三:硅酸钠、碳酸钠和氢氧化钠
【实验探究】

|
实验1 |
实验2 |
实验3 |
|
|
样品质量/g |
50 |
50 |
50 |
|
NaOH溶液质量/g |
20 |
40 |
60 |
|
电子秤读数m/g |
42.45 |
44.9 |
44.9 |
请计算: