小君用溶解硫酸铜固体的方法配制100 g 8%的硫酸铜溶液,具体步骤如下:
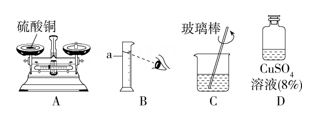
需要硫酸铜固体的质量为g。
Ⅱ.称量
①称量过程中,若发现天平指针偏右,此时应该(填字母),至指针指向标尺中央。
A.调节游码和砝码
B.调节平衡螺母
C.减少硫酸铜固体
D.增加硫酸铜固体
②量取水时,如果按照B的方式读数,会使配制的溶液的溶质质量分数(填“偏大”或“偏小”)。
Ⅲ.溶解
Ⅳ.装瓶,贴标签
Ⅰ.【实验目的】探究溶解过程中,溶液温度的变化情况。
Ⅱ.【查阅资料】
物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
实验条件下,水的凝固点为0 ℃、沸点为100 ℃。
Ⅲ.【提出猜想】物质溶解过程中,溶液的温度可能升高或降低或不变。
Ⅳ.【实验探究】某探究小组的同学设计了如图所示的两种方案。在图乙所示方案中,每次加入物质b之前均使用温度计控制热水温度,使之保持在99 ℃。
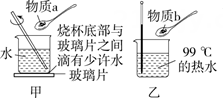
Ⅵ.【拓展实验】按照如图丙所示进行实验。若物质c为NaOH,则U形管内的左边液面将(填“高于”“低于”或“等于”)右边液面。