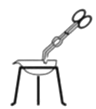
 取下刚加热后的蒸发皿
B .
取下刚加热后的蒸发皿
B .  加入锌粒
C .
加入锌粒
C .  熄灭酒精灯
D .
熄灭酒精灯
D . 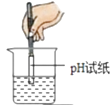 测溶液 pH
测溶液 pH
选项 | 所用试剂 | 现象和结论 |
A | 无色酚酞溶液 | 溶液不变色,则恰好完全反应 |
B | 氯化钡溶液 | 出现白色沉淀,则硫酸过量 |
C | 铜片 | 无气泡产生,则恰好完全反应 |
D | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
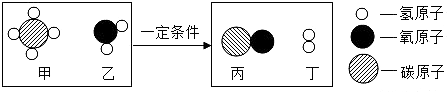
① 空气成分中,含量最多的气体是(用化学式表示),用于填充气球且性质稳定的气 体名称。
② 甲烷可作燃料,其燃烧的化学方程式是。
③ β一胡萝卜素(化学式:C40H56)是一种常见食品添加剂, 0.1mol C40H56 中约含个C40H56 分子(用科学记数法表示)。
水是很好的溶剂。下表是 NaCl 和 KNO3 在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
(g/100g 水) | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |

A 中溶液是(填“饱和”或“不饱和”)溶液,C 中溶液的总质量是g;
a.有 NaCl 晶体析出,无 KNO3 晶体析出
b.两溶液中溶质与溶剂的质量比都增大
c.剩余溶液的质量:NaCl 溶液大于 KNO3 溶液
d.析出 NaCl 晶体 3.7 g
②铁制品在潮湿空气中容易生锈,请写出工业上除铁锈的方法(用化学方程式表示)。
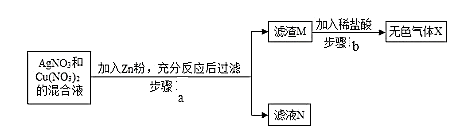
I.步骤 b 中生成的无色气体 X 是,滤液 N 中的溶质是;
II.步骤 a 中发生反应的化学方程式(任写一个即可)。

① 装置 A 中发生反应的化学方程式;装置 B 的作用是; 装置 C 中的现象是。
② 装置 D 玻璃管中发生反应的化学方程式 ,该反应中具有还原性。
③ 装置 E 的作用是 ,本实验还应在装置之间添加装置 E。
④ 从保护环境的角度分析,本实验的不足是。
⑤ 从微观角度分析 CO2 与 CO 化学性质不同的原因是。

① 碳酸钠是一种重要的盐,甲中碳酸钠溶液中加入酚酞,溶液显色;乙和丙中都能观察到的实验现象是;乙中发生反应的化学方程式是, 该反应属于发应(填基本反应类型);
② 实验结束后,将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并 呈红色;静置,取上层清液于试管中,加入过量氯化钡溶液,有白色沉淀,溶液呈红色。 则废液缸中的废液一定含有指示剂、水、碳酸钙、; 在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑。
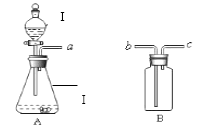
①仪器I的名称是,若A装置内药品为Zn和稀盐酸,反应的化学方程式为;若B装满水,用于收集A生成的H2 , 则a接(填“b”或“c”)。
② 实验室用 A 制 O2 的原理是(用化学方程式表示)。
③ 装置 B 收集 CO2 , 验满时,燃着木条应放在(填“b”或 “c”)端。
④ 将实验室制得的 CO2 通入澄清石灰水,石灰水未变浑浊,作如图探究:
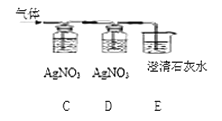
完成填空:
装置C、E 中溶液变浑浊,D 中溶液不变浑浊,则原石灰水未变浑浊的原因是, 装置 D 的作用是,E 中石灰水变浑浊的原因是(用化学方程式 表示)。
⑤ 实验室制 CO2 , 若有 0.4mol 碳酸钙完全反应,求生成二氧化碳的质量。(根据化学方程式列式计算)