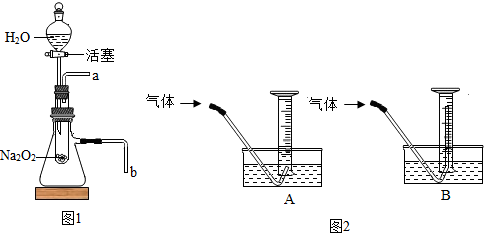
(猜想与假设)对生成的气体成分进行判断,他提出了以下三种假设:
A.该气体是CO2
B.该气体是O2
C.该气体是H2
(实验验证并得出结论)
立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠。
通过查阅资料,同学们又得知:在化学反应中,有元素化合价升高,就必然有元素化合价降低。于是通过小组讨论,大家一致认为上述假设中的(填“A”或“B”或“C”)肯定也不合理。
|
操作步骤 |
实验现象 |
结论 |
|
取少量固体粉末于试管中,打开活塞使水流入试管,将带火星的木条放在图1中的导管(填“a”或“b”)处 |
带火星木条复燃 |
证明是该气体是O2 |
小王同学用图2装置,测量生成氧气的体积;测量气体体积读数时,必须待试管和量筒内的气体都冷却至室温时才能进行,因此应选用图2装置中的(填“A”或“B”),否则测量结果会(填偏大”或“偏小”)。