步骤1.称取4.0g碎铁屑,放入烧杯中,加入10%Na2CO3溶液,煮沸、水洗至中性。
步骤2.向清洗后的碎铁屑中加入3mol/L H2SO4溶液20mL,盖上表面皿,放在水浴中加热。不时向烧杯中滴加少量蒸馏水,控制溶液的pH不大于1。
步骤3.待反应速度明显减慢后,趁热过滤得FeSO4溶液。
①步骤1的实验目的是。
②步骤2“不时向烧杯中滴加少量蒸馏水”的目的是;“控制溶液的pH不大于1”的目的是。
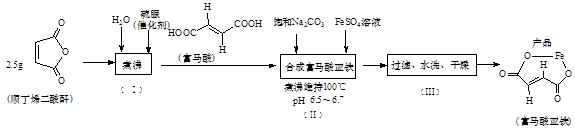
①步骤(Ⅰ)所得产品(富马酸)为-丁烯二酸(填“顺”或“反”)。
②富马酸与足量Na2CO3溶液反应的方程式为。
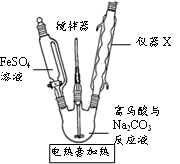
③图中仪器X的名称是,使用该仪器的目的是。
①(NH4)2Ce(SO4)3标准溶液适宜盛放在(填“酸式”或“碱式”)滴定管中。
②该实验中能否用KMnO4标准溶液代替(NH4)2Ce(SO4)3标准溶液滴定Fe2+ , 说明理由。
③产品中铁的质量分数为(用含a、V的代数式表示)。