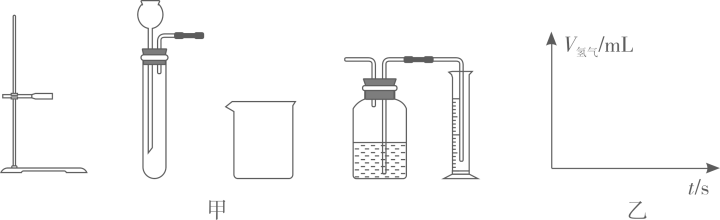
①检查装置气密性:连接试管和广口瓶,往漏斗中加水,液面(选填“持续下降”或“不持续下降”),说明装置的气密性好;
②装药品:在烧杯中加入碎冰和一定量的水。在试管中装入锌粒,把试管放入烧杯内的冰水中。之后的重复实验,也都在冰水混合物中进行,是因为。而后用铁架台把试管固定,再连接好其他装置;
③开始反应和测量:打开止水夹,往漏斗中倒入一定量的2%稀盐酸,量筒中的水量不再变化时,记录水的量,这个量就是反应得到的气体的量,此处使用了转化法的科学方法;
④取等量的锌粒与4%和6%稀盐酸进行反应,重复上述实验;
⑤取铁片代替锌粒进行反应,重复上述实验。重复实验的目的。