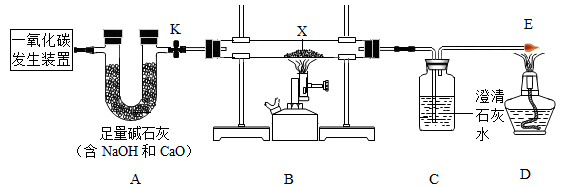
A装置的作用是。
(查阅资料)
①碳还原氧化铜时,在一定条件下反应生成铜,或同时生成少量的氧化亚铜(Cu2O);
②Cu2O和Cu都为红色固体,且Cu2O能与稀硫酸反应,反应的化学方程式为 .
(实验探究)按上图装置进行实验(关闭活塞k)。
取一定质量比的木炭粉和氧化铜的混合物放入X处进行实验,观察到黑色粉末变为红色,经检验红色固体为铜,则X处发生反应的化学方程式为。
|
实验操作 |
实验现象 |
实验结论 |
结论解释 |
|
|
溶液变蓝色有红色固体 |
|
|
(实验结论)一定条件下,碳能还原氧化铜且反应物比例不同,可能生成物不同。