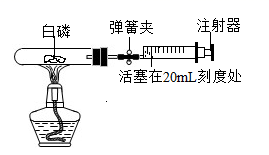
①开始实验前,该小组同学打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处。该操作的主要目的是。
②实验后,可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约处。
a.4mL刻度
b.8mL刻度
c.12mL刻度
d.16mL刻度
③下列实验操作,对实验结果有影响的是。
a.装置漏气
b.白磷过量
c.燃烧结束后,立即松开弹簧夹,观察现象
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小婧查阅资料, 记录了下列几种物质的颜色:
|
物质 |
MgO |
MgCl2 |
Mg3N2 |
Mg( NO3)2 |
Mg( OH)2 |
|
颜色 |
白色 |
白色 |
淡黄色 |
白色 |
白色 |
[初步分析]其他同学认为不可能生成上表中的,理由是。
[提出猜想]分析资料,小婧认为淡黄色固体可能是由镁与空气中的反应生成的。
[实验探究]小婧设计实验证实了自己猜想。
[实验结论]根据小婧的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:;。
[反思与评价]①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2 , 为什么呢?请给出合理的解释。
②通过上述实验,你对燃烧有什么新的认识?。