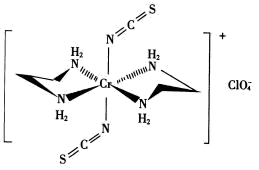
①阴离子 的空间构型为形。
②配离子中,中心离子的配位数为,N与中心原子形成的化学键称为键。
③配体H2NCH2CH2NH2(乙二胺)中碳原子的杂化方式是,分子中三种元素电负性从大到小的顺序为。

图1中F和O共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为,晶体密度ρ=g·cm−3(用含x的表达式表示,设阿伏加德罗常数的值为NA)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标( ),则原子2的坐标为。