(提出问题)金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
|
实验编号 |
盐酸的浓度(均取20mL) |
温度/℃ |
记录的数据 |
|
① |
5% |
30 |
|
|
② |
10% |
20 |
|
|
③ |
5% |
20 |
|
|
④ |
10% |
30 |
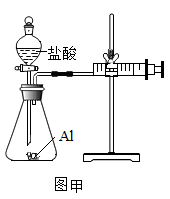
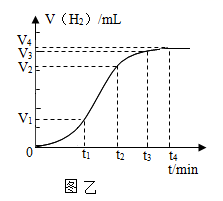
(交流讨论)
①请写出铝与稀盐酸反应的化学方程式。
②实验前小明检查图甲装置的气密性的方法是。
实验中记录的数据可能是;对比实验②③可知对金属与酸反应的速率的影响。
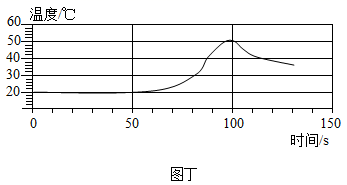
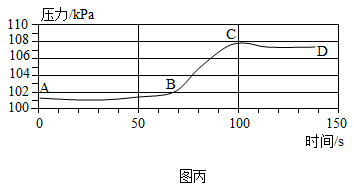
图丁中0-50秒的时间温度无明显变化的可能原因是,CD段气体压力逐渐下降的原因是。