①移取待测的盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞
②用标准溶液润洗碱式滴定管2~3次
③把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴部分充满溶液
④取标准溶液注入碱式滴定管至0刻度以上
⑤调节液面至0或0刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准溶液滴定至终点,记下滴定管液面的刻度
回答以下填空:
正确操作的顺序是(填序号)②→→→①→。
某实验室有瓶混有泥沙的乙二酸样品,欲测定样品中乙二酸的含量。准确称量
乙二酸样品,配成
溶液。量取
所配溶液于锥形瓶中,加少量硫酸酸化,将
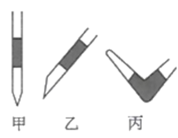
溶液装入(填“酸式”或“碱式”)滴定管,进行滴定操作,当时,证明达到滴定终点。
序号 | 滴定前读数( | 滴定后读数( |
1 | 0.00 | 20.10 |
2 | 1.00 | 20.90 |
3 | 0.00 | 22.10 |
则此样品的纯度为。