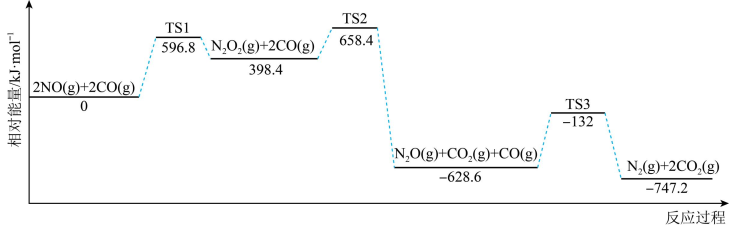
①反应过程中速率最慢步骤的热化学方程式为,活化能最小。
②为提高NO的平衡转化率可采用的措施为(填标号)。
A.升高温度 B.增大压强 C.增大NO浓度 D.使用催化剂
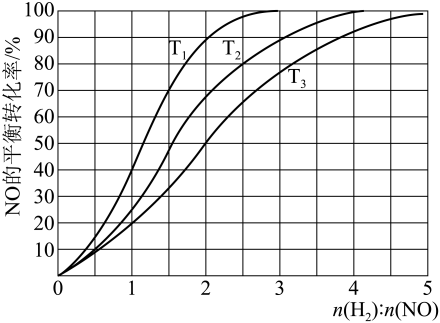
①应温度、
、
从大到小的关系为。
②温度下,充入
、NO分别为3mol、3mol,容器内的压强为w Pa,反应进行到10min时达平衡,0~10min内
的平均反应速率为。该反应的平衡常数
(写出计算表达式,以分压表示的平衡常数为
, 分压=总压×物质的量分数)。
③该反应的正反应速率方程可表示为 ,
下测得有关数据如下表:
NO/mol | v正/mol·L-1·min-1 | |
1 | 1 | 4.14k |
1 | 4 | 16.56k |
2 | 1 | 16.56k |
则,
。