【实验资料】
①Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢H2S(水溶液呈酸性)。
②硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液、空气中各成分均不反应。
【实验过程】
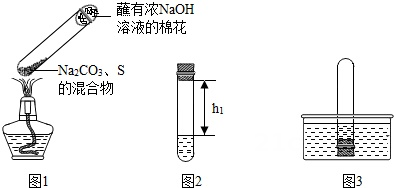
①取碳酸钠、硫粉混合后置于试管中,加热(如上图1所示,夹持装置已略去),制得Na2S4 , 反应为4Na2CO3+12S+O2═2Na2S4+2Na2S2O3+4CO2 , 蘸有浓NaOH溶液的棉花的作用是。
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据h1(如图2所示)
③将该试管插入水中(如图3所求),按下橡胶塞,观察到现象为
再塞紧橡胶塞。将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据h2 , 理论上h1:h2=
④若实验过程中②中,取下棉花后,未放置一段时间即进行后续操作,会导致测量的空气中的氧气的体积分数(选填“偏大”,“偏小”或“不影响”)。