Ⅰ.某实验小组设计了如图在纽扣上电镀铜的实验装置:
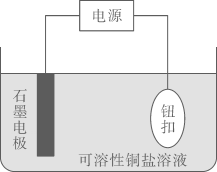
装置示意图 | 序号 | 电解质溶液 | 实验现象 |
| ① | 0.1mol/L | 阴极表面有无色气体,一段时间后阴极表面有红色固体,气体减少。经检验,铁电极表面有 |
② | 0.1mol/L | 阴极表面未观察到气体,一段时间后阴极表面有致密红色固体,经检验,电解液中无Fe元素。 |
实验①中,无色气体产生的原因是或。
微信扫码预览、分享更方便