1.
(2023高二上·仁怀期中)
科学家利用CO2和H2合成CH3OH有利于实现碳中和。主要反应有:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g),ΔH1=-49.4kJ·mol-1
CH3OH(g)+H2O(g),ΔH1=-49.4kJ·mol-1
II.CO2(g)+H2(g) CO(g)+H2O(g),ΔH2
CO(g)+H2O(g),ΔH2
III.CO(g)+2H2(g) CH3OH(g),ΔH3=-90.6kJ·mol-1
CH3OH(g),ΔH3=-90.6kJ·mol-1
回答下列问题:
-
(1)
ΔH2=kJ·mol-1 , 反应III在(填“高温”或“低温”)易自发进行。
-
-
(2)
若将反应I看成由反应II和反应III两步进行,反应II为慢反应,画出由反应原料经两步生成产物的反应过程能量示意图
。

-
-
(3)
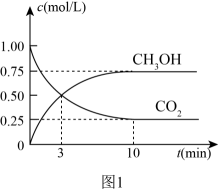
一定条件下,在体积为1L的密闭容器中发生反应I,起始物n(H
2)/n(CO
2)=3,CO
2(g)和CH
3OH(g)的浓度随时间变化如图1所示,3min内用H
2浓度变化表示的反应速率
mol·L
-1·min
-1。若平衡时压强为P
0 , 该反应条件的平衡常数K
p=
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
-
-
(4)
反应II中,为提高H2的转化率,可采取的措施有(任意答一条)。
-
-
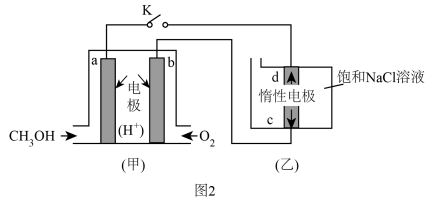
(5)
图2是以甲醇燃料电池为电源电解饱和食盐水,甲装置a电极反应式为
。当甲装置中消耗11.2LO
2(标准状况),理论上乙装置中通过导线的电子数目为
。
-
CH3OH(g)+H2O(g),ΔH1=-49.4kJ·mol-1
CO(g)+H2O(g),ΔH2
CH3OH(g),ΔH3=-90.6kJ·mol-1


