1.
(2023九上·浙江模拟)
科学实验拓展课上,小明用如图甲所示的装置(部分固定用装置未画出)测定石灰石中CaCO3的含量在锥形瓶中加入5.0g石灰石,通过分液漏斗逐滴加入足量盐酸,经计算,最终得到CO2气体1.76g。然后将一定量的CO2通入某NaOH溶液后,再往溶液中逐滴加入80mL3.65%的稀盐酸(密度为1.0g/mL),生成CO2的质量与加入盐酸的体积关系如图乙所示。
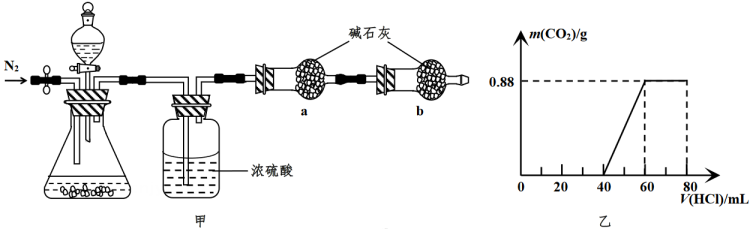
已知:①往NaOH溶中缓慢通入CO2至过量的反应依次为:
2NaOH+CO2=Na2CO3+H2O,NaCO3+CO2+H2O=2NaHCO3
②Na2CO3溶液中逐滴加入称盐酸的反应分为2步,依次为: Na2CO3+HCl=NaHCO3+NaCl,
NaHCO3+HCl=NaCl+CO2↑+H2O。
-
(1)
测定石灰石中CaCO3含量实验中,小明通入N2的作用是。
-
-
(2)
求小明用来制取CO2的石灰石中碳酸的质量分数。
-
-
(3)
根据图乙可知,往NaOH溶液中通入一定量的CO2后,溶液中的溶质为。
-
-
(4)
将加入80mL稀盐酸后的溶液蒸干,得到固体的质量是多少?
-
