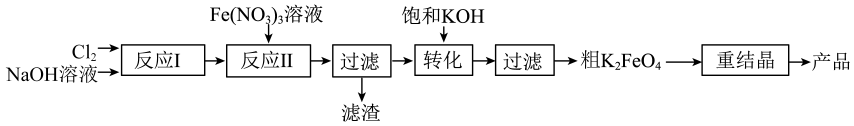
用以下装置可以完成上述反应I和反应Ⅱ:
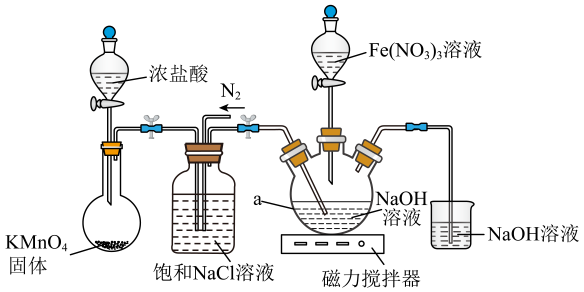
信息:①易溶于水,微溶于KOH溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液中快速产生
;在0~5℃碱性溶液中较稳定。
②部分物质在水中的溶解度见下表
物质 | 溶解度/g | |||
10℃ | 20℃ | 30℃ | 80℃ | |
NaCl | 35.8 | 36.0 | 36.3 | 38.4 |
80.0 | 88.0 | 96.0 | 148.0 | |
()→()→()→置于冰水浴中→()→用乙醇洗涤→干燥→得产品
a.将粗产品溶于水b.将粗产品溶于冷的稀KOH溶液 c.过滤取沉淀
d.过滤取滤液e.蒸发浓缩,趁热过滤f.加入饱和KOH溶液g.冷却结晶
称取ag左右碘化钾于碘量瓶中,加入100mLNaOH溶液和bg左右的固体氟化钠,待溶解完毕;准确称取mg样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
标准溶液进行滴定,消耗标准液体积为VmL。已知:
,
(方程式未配平)
①本次实验测得纯度为,然后重复上述过程,平行测试3次。
②实验过程中往往需要加入过量且比理论计算所需量过量2~3倍左右的KI,理由是。