1.
(2024九上·德庆期末)
某金属冶炼厂用炉甘石(主要成分为ZnCO3)为原料冶炼金属锌。学校兴趣小组为了测定炉甘石中ZnCO3的质量分数,进行了以下探究:
【查阅资料】ZnCO3与CaCO3性质类似,与盐酸反应生成氯化锌、水和二氧化碳。
往装有30g炉甘石样品的烧杯中分次加入稀盐酸(杂质不参与反应),每次都在溶液中不再产生气泡时称量,所得数据如下表:
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
测得产生的总质量/g | 2.2 | X | 6.6 | 8.8 | 8.8 |
请回答并计算:
-
(1)
上表中X=;炉甘石中的ZnCO3完全反应时,共需要盐酸g。
-
-
(2)
炉甘石样品中碳酸锌的质最分数为多少?(写出计算过程,精确到0.1%)。
-
-
(3)
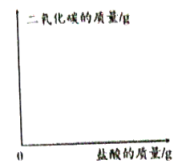
分析实验数据,在“题21图”中,画出加入盐酸过程中,产生二氧化碳质量对应的变化图,并标注必要的数值。
-
