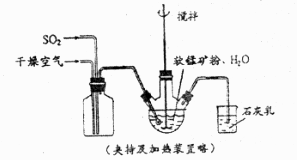
①缓慢向烧瓶中(见上图)通入过量混合气进行“浸锰”操作,主要反应原理为:
(铁浸出后,过量的
会将
还原为
)
②向“浸锰”结束后的烧瓶中加入一定量纯 粉末。
③再用 溶液调节pH为3.5左右,过滤。
④调节滤液pH为6.5-7.2,加入 ,有浅红色沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。
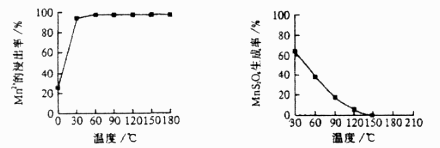
图1 温度对锰浸出率的影响 图2 浸锰温度与 生成率的关系
表1:生成相应氢氧化物的pH
物质 | ||||
开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |