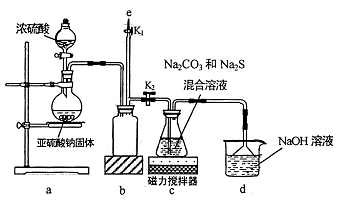
实验中要控制SO2生成速率,可采取的措施有(写出一条)。
已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-=[Ag(CN)2]- , Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
①滴定时1.00×10-4mol/L的标准AgNO3溶液应用(填仪器名称) 盛装; 滴定终点时的现象是。
②处理后的废水是否达到排放标准(填“是”或“否”)。