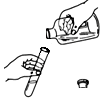
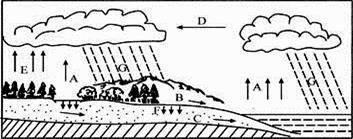
 B .
B . 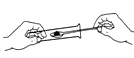 C .
C . 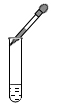 D .
D . 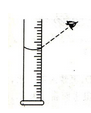
A. | B. | C. | D. | |
面料 | × | × | √ | √ |
油污 | × | √ | × | √ |
①若用氢氧化钠固体配制,需称取氢氧化钠固体7.0g
②用托盘天平称氢氧化钠固体时,在两盘各放一只质量相等的烧杯
③选用200mL量筒量取所需水的体积
④实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
⑤用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小.

选项 | 混合物的分离或提纯 | 分离物质的原理 |
A | 除去粗盐中的泥沙 | 氯化钠和泥沙的溶解性不同 |
B | 将石油分馏得到石油产品 | 石油中各成分的密度不同 |
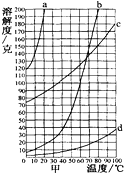
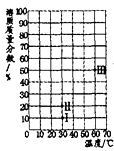
C | 分离硝酸钾和氯化钠组成的混合物 | 硝酸钾和氯化钠分解温度不同 |
D | 分离液态空气制取氧气 | 利用氮气和氧气的熔点不同 |
 B .
B .  C .
C . 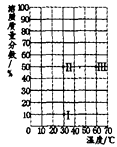 D .
D . 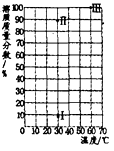
|
|
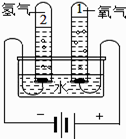
图1.水的电解 | 图2.电解水的微观示意图 |
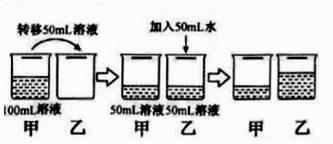
①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
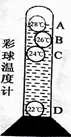
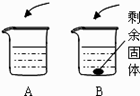
①溶解 ②称量和量取 ③计算 ④装入试剂瓶贴好标签
配制上述溶液正确的实验步骤顺序是(填序号)。
①把1.0g药品溶于水配制成4.0mL溶液a
②取0.1mL溶液a,加水稀释至1.0mL,得溶液b
③取0.1mL溶液b,加水稀释至1.0mL,得溶液c
④取0.4mL溶液c,加水稀释至1.0mL,得溶液d
由于在整个配制过程中药液很稀,其密度都可近似看做1g/cm3。则最终得到的药液(溶液d)中溶质的质量分数为。

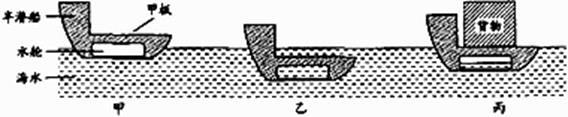
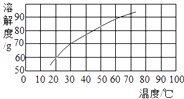
⑴室温为20℃,氯化钠的溶解度为36g。计算要溶解5g粗盐,至少需要加水的质量是。
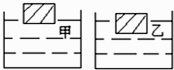
⑵粗盐溶解后要过滤,选用的装置是(填“A”或“B”);过滤之后澄清溶液中含有的溶质是。
⑶蒸发
⑷计算产率:用玻璃棒将所得精盐转移到纸片上,称量其质量为3.8g,则精盐产率是
( )小明觉得产率偏低,请你帮他分析原因,写出一点即可:。
浓硫酸(H2SO4) 500毫升 | |
浓度(质量分数) | 98% |
密度 | 1.84克/厘米-3 |
相对分子质量 | 98 |
强腐蚀性,阴冷,密封贮藏 | |
①以小明家平均每天使用15次计算,每天可节约用水多少千克?
②洁具正常情况下使用时间可达十多年。若节水型洁具价格为600元,而普通型洁具价格为300元,水费平均为3元/吨,试通过计算说明小明家购买节水型洁具是否划算?(每月按30天计算)
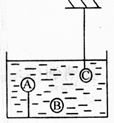
金属 | 金 | 铜 | 铁 | 铝 |
密度(×103kg/m3 | 19.3 | 8.9 | 7.9 | 2.7 |