

| 选项 | 实验目的 | 实验操作 |
| A | 鉴别蒸馏水和稀氯化钾溶液 | 蒸发至干 |
| B | 鉴别空气、O2、CO2和H2 | 分别伸入燃着的木条 |
| C | 比较空气与呼出气体中CO2含量 | 分别伸入燃着的木条 |
| D | 证明不同金属与酸反应的剧烈程度不同 | 将铜和银分别放入稀盐酸中 |
2017年5月18日,我国宣告可燃冰试采成功,这在世界上也是首次。“可燃冰”是天然气和水在低温、高压条件下形成的冰状固体,遇火即可燃烧。可燃冰外观像冰,在地球上的储量大约是已探明其他化石然料总量的2倍;同等条件下,可燃冰燃烧产生的能量比传统的化石燃料要多岀数十倍,而且燃烧后不产生仼何的残渣和废气,是公认的地球上尚末开发的最大新型能源。
A.储量丰富
B.燃烧值大
C.清洁、无污染
D.易于开采
①称量氯化钠固体的质量为g;
②下列仪器中必须使用的是(填序号)。
A.托盘天平
B.烧杯
C.玻璃棒
D.10mL量筒 E.50mL量筒

①甲、乙两种物质中溶解度受温度影响较大的是物质。
②若将t2℃时甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法。(填一种即可)
③若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是。
④t1℃时,若将25g乙固体加入50g水中,充分搅拌后,仍有9.2g乙固体未溶解,则t1℃时乙的溶解度为。
⑤t2℃接近饱和的甲溶液逐渐冷却至t1℃,图2中有关量随时间变化的趋势正确的是。(选序号)
A.在干燥的空气中
B.在潮湿的空气中
C.浸没在植物油中
D.部分浸入食盐水中
写出一种防止铁制品生锈的具体方法:。

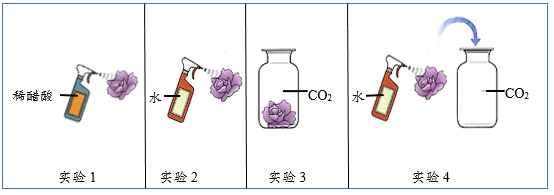

①密度大于空气②难溶于水③密度比空气小
