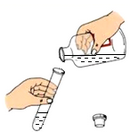
 倾倒液体
B .
倾倒液体
B . 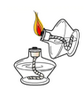 点燃酒精灯
C .
点燃酒精灯
C . 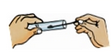 取用固体粉末
D .
取用固体粉末
D . 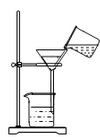 过滤
过滤
 B .
B .  C .
C .  D .
D . 

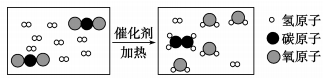
 B . H2O和H2O2中氢元素的化合价相同
C . 电解水实验中氢气和氧气的质量比为2:1
D . 水沸腾时可冲起壶盖,说明温度升高水分子变大
B . H2O和H2O2中氢元素的化合价相同
C . 电解水实验中氢气和氧气的质量比为2:1
D . 水沸腾时可冲起壶盖,说明温度升高水分子变大
| 序号 | 实验事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 大块木头不易点燃,而刨成非常薄的片状却易点燃 | 反应物的种类 |
| D | 双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解 | 有、无催化剂 |

①氧气在通常情况下是无色无味的气体;
②氧气不易溶于水;
③在标准状况下氧气的密度是1.429g/L比空气重;
④将纯氧吹入炼钢炉中,可以提高炉温,用于炼钢;
⑤氧气在一定条件下能与铁丝、木炭等物质发生化学反应;
⑥氧气具有氧化性.其中属于物理性质的是,属于化学性质的是,属于用途的是.

A+E→B
D→B+C


请写出过氧化氢分解的化学方程式:,
(查阅资料)①.过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②.温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
|
序号 |
实验步骤 |
实验现象 |
实验结论 |
|
① |
分两次进行实验,均注入5mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 |
量筒中2分钟收集到的气体体积均为5mL |
猜想不成立 |
|
② |
分两次进行实验 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液 第二次 |
第一次,量筒中2分钟收集到的气体体积为56mL 第二次,量筒中2分钟收集到的气体体积为5mL |
猜想成立 |
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
|
加入过氧化氢酶 |
不加过氧化氢酶 |
|||||
|
反应温度/℃ |
25 |
37 |
42 |
25 |
37 |
42 |
|
收集到气体体积/mL |
39 |
56 |
60 |
5 |
5 |
5 |
通过这些数据,你能得出的新结论是。
要证明某物质是催化剂,还需要证明的是。

|
反应前,整套装置+样品的质量/g |
共加入:稀盐 酸的质量/g |
反应后,整套装置+锥 形瓶中剩余物的质量/g |
|
104.60 |
20.00 |
123.72 |