 B . 加热液体
B . 加热液体  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 测溶液的pH
D . 测溶液的pH 
 D .
D . 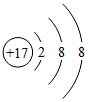
① | ② | ③ | ④ | ⑤ | |
X | 稀盐酸 | 水 | 水 | 双氧水 | 水 |
Y | 铁粉 | 氢氧化钠 | 氯化钠 | 二氧化锰 | 硝酸铵 |



①向氢氧化钠溶液中逐滴加入稀盐酸
②向一定量的碳酸钙固体中逐滴加入稀盐酸至过量
③一定温度时,将饱和的氯化钠溶液恒温蒸发至有晶体析出
④将足量的金属镁片和锌片分别与等质量的相同质量分数的稀硫酸混合
A.紫砂锅  B.陶瓷碗
B.陶瓷碗  C.不锈钢水瓢
C.不锈钢水瓢  D.塑料盆
D.塑料盆 


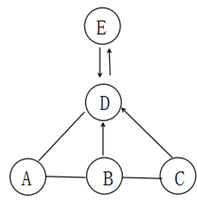
该反应属于。(填基本反应类型)

(提出问题)导致溶液碱性减弱的原因是什么?
(假设与分析)
假设1:可能是氢氧化镁与N2或O2发生了反应。
假设2:可能是溶液吸收了空气中的。
假设3:可能是氢氧化镁的溶解度随温度的降低而。
由碱的性质可知,假设1不成立。
(实验探究)
|
实验操作 |
实验现象 |
结论 |
|
Ⅰ.取上述紅色溶液,保持温度不变,在空气中放置一段时间,观察现象。 |
① |
假设2成立 |
|
Ⅱ.取上述红色溶液,②,③观察现象。 |
红色褪去 |
假设③成立 |
将一小块金属钠投入硫酸铜溶液时,产生蓝色沉淀。
请解释其原因:。