 B .
B .  C .
C .  D .
D . 
 贮存呼出的气体
B .
贮存呼出的气体
B .  点燃酒精灯
D .
点燃酒精灯
D .  稀释浓硫酸
稀释浓硫酸
| A.性质用途 | ①氮气化学性质不活泼,可用作保护气 ②氧气具有可燃性,可用作燃料 |
| B.安全生活 | ①室内放一盘水可以预防 CO 中毒 ②新装修的房屋要通风一段时间后再入住 |
| C.宏观微观 | ①热胀冷缩是由于分子间隔随温度而变化 ②水电解是化学变化,其中水分子发生了改变 |
| D.健康安全 | ①若出现贫血,可适当补充铁元素 ②霉变的大米清洗煮熟后,可继续食用 |
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | |

| 选项 | 实验操作 | 现象 | 结论 |
| A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 说明黄铜的硬度比铜大 |
| B | 用小木棍蘸少量浓硫酸 | 木棍变黑 | 浓硫酸有吸水性 |
| C | 向 Na2CO3溶液中滴入酚酞溶液 | 溶液变红 | 碳酸钠是碱 |
| D | 用燃着的木条伸进某瓶气体中 | 木条熄灭 | 该气体一定是CO2 |
 B . 向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸
B . 向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸  C . 向一定质量分数的盐酸中不断加水
C . 向一定质量分数的盐酸中不断加水  D . 一定质量的碳粉与过量的氧气在密闭容器中充分反应
D . 一定质量的碳粉与过量的氧气在密闭容器中充分反应 


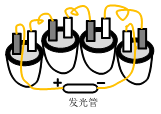



①在A装置中观察到的现象,证明氢氧化钠与二氧化碳确实发生了反应。
②实验后进入A装置中的溶液明显多于C装置,此现象还能验证氢氧化钠和氢氧化钙的性存在较大差异,所以,实验室吸收二氧化碳用氢氧化钠而不用氢氧化钙。
|
混合物质 |
B+C |
C+D |
D+E |
|
现象 |
产生气体 |
产生沉淀 |
产生沉淀 |

资料:NH4Cl溶液显酸性,且浓度越高酸性越强

a.称取14.7gCaCl2•xH2O晶体于锥形瓶内,加入适量蒸馏水。使其全部溶解。
b.再向其中加入足量的Na2CO3溶液,静置。
c.过滤、洗涤、干燥、称量,得到10.0g固体。
①判断该步骤b中沉淀是否完全的方法是:静置,取少量上层清液,滴加溶液,若没有沉淀产生,则说明已沉淀完全。
②CaCl2•xH2O中,x=。
|
内容 |
| | 溶液③是 |
| 现象 | 有气泡产生 | 现象是。 | 溶液由红色恰好变成无色 |
| 实验 解析 | 化学方程式是。 | 化学方程式: H2SO4+Ba(NO3)2=BaSO4↓+2HNO3 | 图中“?”代表的离子是 (填离子符号)。 |
| 结论 | 生成物中有气体或有或有水生成时,复分解反应可以发生。 | ||

无色溶液B的pH7(填“<”、“>”或“=”)。

A反应后溶液的总质量
B参加反应的氯化钙质量
C氯化钙溶液中溶质的质量分数
D恰好完全反应时,溶液中氯化钠的溶质质量分数
