



| 选项 | 实验目的 | 所用试剂或操作方法 |
| A | 鉴别稀盐酸、Na2CO3溶液和蒸馏水 | 分别滴加无色酚酞溶液,观察颜色 |
| B | 除去生石灰中少量的碳酸钙 | 加水溶解,过滤 |
| C | 验证Zn、Cu、Ag的金属活动性 | 将铜片分别放入到Zn(NO3)2溶液、AgNO3溶液中,观察现象 |
| D | 除去CO2中混有少量的HCl气体 | 将气体通入足量的NaOH溶液 |
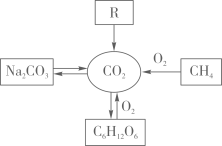
制取CO2:……………
制取Cl2:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
已知:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。

①写出图中仪器Ⅱ的名称是;
②用D装置收集Cl2时,Cl2应从管口(填导气管接口处的字母)进入瓶中。
③用A装置制取氧气后,从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是。
(查阅资料)
①蚁酸化学名称叫甲酸,化学式为HCOOH
②蚁酸在一定条件下会分解生成两种氧化物
③白色无水硫酸铜粉末遇水变蓝
(提出问题)蚁酸的酸碱性及分解产物是什么?
猜想①:蚁酸的分解产物是水和二氧化碳;
猜想②:蚁酸的分解产物是水和一氧化碳;
猜想③:蚁酸的分解产物是一氧化碳和二氧化碳。
经讨论,小组同学认为猜想③是错误的,理由是。
探究蚁酸的酸碱性。
用pH试纸测得蚁酸溶液的pH值7(填“>、<或=”),证明蚁酸溶液呈酸性。

为了确认蚁酸分解的所有产物,小组同学设计实验,将蚁酸分解的产物通入下图所示的实验装置,并观察现象。
(现象与结论)
实验中观察到A中无水硫酸铜变蓝,B中澄清石灰水未变浑浊,D中黑色粉末逐渐变红, E中澄清的石灰水变浑浊。
写出E中发生的反应的化学方程式;
通过对实验现象的分析,上述猜想正确。
从环保的角度考虑,上述实验装置设计上存在的不足之处是。
人们被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒,下列物质中你会选择的物质是。
A NaOH溶液 B 食醋 C 食盐水 D 肥皂水
|
烧杯质量 |
样品的质量 |
稀盐酸的质量 |
烧杯+剩余物的总质量 |
|
50g |
5.8g |
94.6g |
150.2g |
注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算: