




|
反应时间/秒 |
0 |
10 |
20 |
30 |
40 |
|
总质量/克 |
310.0 |
309.6 |
308.6 |
307.8 |
307.8 |
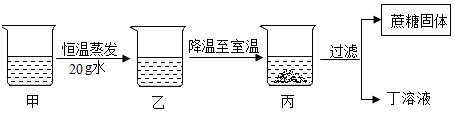
完全反应后,生成的CO2气体的质量为克。
实验次数 | 1 | 2 | 3 | 4 |
稀硫酸的用量/克 | 20 | 20 | 20 | 20 |
剩余固体的质量/克 | 20.0 | 17.4 | 14.8 | 13.5 |
分析上述数据,请回答下列问题:

①去掉装置A,将空气直接鼓入装置B
②去掉装置C,将B与D装置直接相连
③当气泡停止产生时立即停止鼓入空气
|
放置时间(小时) |
烧杯中物质减小的质量(克) |
|||
|
水 |
饱和氯化钠溶液 |
饱和硝酸钾溶液 |
7.3%的稀盐酸 |
|
|
24 |
1.85 |
0.61 |
0.72 |
1.35 |
|
48 |
3.70 |
? |
1.44 |
2.80 |
请回答:
通过计算,确定散口放置48小时的稀盐酸溶质质量分数是“变大”、“变小”还是“不变”?并对变化的原因作出解释。

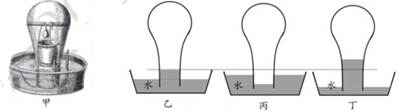
实验一:将6个盛有等量澄清石灰水的敞口容器固定在铁丝上,点燃蜡烛,立即用小玻璃罩罩上(如图乙),分别记下各容器内石灰水变浑浊所需的时间。多次重复实验获得数据如表。
容器编号 | 1 | 2 | 3 | 4 | 5 | 6 |
平均时间/秒s | 3.2 | 3.8 | 5.0 | 7.1 | 11.1 | 19.0 |
实验二;将3支温度计分别挂在小玻璃罩内不同位置(如图丙),点燃蜡烛,一段时间后发现温度计①示数明显增大,温度计②③示数增大不明显。
猜想一:可能是CaCO3和Fe;
猜想二:可能是CaCO3和Fe2O3;
猜想三:可能是 。
【实验设计】小明设计了下图所示的实验;
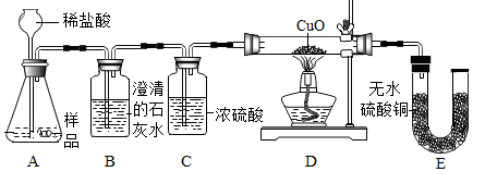
【实验与分析】
⑴向A装置中加入稀盐酸,B装置中出现浑浊现象,证明样品中含有CaCO3。
⑵若粉末中含有Fe,装置E中应观察到的现象是。
【评价与反思】
上述实验中,如果将E装置去掉,是否还能验证粉末中含有Fe,请说明理由 。
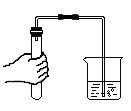
Ⅰ.将一根长度等于玻璃钟罩最宽部分直径的铁棒横放在钟罩里,把装有稀硝酸的陶罐通过铁钩挂在铁棒上,用绳索将小铁方(铁块的升降通过在钟罩外拉动或放松绳索来实现)。
Ⅱ.调整水槽中初始水位如图乙,再使铁块浸入稀硝酸中,观察到铁块表面迅速产生大量气泡,钟罩内水面下降。[稀硝酸有强氧化性,能与铁发生如下反应:4HNO3+Fe=Fe(NO3)3+NO↑+2H2O]
Ⅲ.当水位降至接近钟罩口时(如图丙),立即取出铁块,以防气体外逸。
IV.等待一段时间后,水面稳定在如图丁的位置。(一氧化氮会与氧气等物质发生如下反应:4NO+3O2+2 ? =4HNO3)
分析与评价:
【提出问题】锡纸中的金属是什么?
【建立猜想】根据锡纸有银白色金属光泽,并结合金属活动性、价格等因素,猜想其中的金属可能是锌、铁、铝、锡中的一种。
【探究过程】
|
步骤 |
活动内容 |
收集证据 |
分析并得出结论 |
|
步骤一 |
①查阅资料:金属锌在室温下很脆 ②取锡纸反复折叠 |
锡纸未破损 |
锡纸中金属不是锌 |
|
步骤二 |
用磁铁靠近锡纸 |
锡纸没有被磁铁吸引 |
锡纸中金属不是 |
|
步骤三 |
①取锡纸条放入浓度为20%的盐酸中除去可能存在的氧化膜。当观察到现象时,取出锡纸条并用蒸馏水清洗。 ②将处理过的锡纸条放入试管中,加入饱和硫酸锌溶液,静置观察。 |
②中锡纸条表面无明显现象 |
说明锡纸中的金属活动性比锌弱,则锡纸中金属不是铝,而是锡 |
【交流评价】小科对实验结论提出质疑:“无明显现象”并不代表没有发生反应,因为铝与硫酸锌反应[2Al+3ZnSO4=3Zn+Al2(SO4)3]生成的金属锌为银白色,与铝颜色相同,因此无法得出结论。请在不改变反应原理的前提下运用定量方法完善实验方案,并根据预期结果得出相应结论: 。
【继续探究】运用完善后的方案进行实验,分析实验结果,得出初步结论:锡纸中金属是铝。
①往盛有另一份混合液的试管中,加入足量的镁片;
②,加入等量的镁片。