 加热液体
B .
加热液体
B .  检查装置气密性
C .
检查装置气密性
C .  检验二氧化碳是否集满
D .
检验二氧化碳是否集满
D .  除去水中的泥沙
除去水中的泥沙



| | 序号 | ① | ② | ③ | ④ | ⑤ |
| 固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
| 固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
| 水的质量/g | 100 | 100 | 100 | 100 | 100 |
下列关于①~⑤所得溶液的说法错误的是( )
 B .
B . 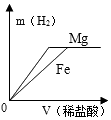 C .
C .  D .
D . 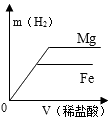
 蓄电池放电
B .
蓄电池放电
B .  水力力电
C .
水力力电
C .  太阳能供热
D .
太阳能供热
D .  火箭点火升空
火箭点火升空
A海水 B冰水混合物 C自来水 D河水


|
实验编号 |
温度/℃ |
大理石规格 |
盐酸的质量分数 |
完全反应的时间/s |
|
a |
20 |
粗颗粒 |
18.25% |
130 |
|
b |
粗颗粒 |
9.125% |
205 |
|
|
c |
30 |
粗颗粒 |
18.25% |
63 |
|
d |
20 |
细颗粒 |
18.25% |
95 |
(实验目的)
①实验a和b探究大理石颗粒大小相同下盐酸的质量分数对该反应速率的影响,则实验b中的温度应该为。
②实验a和c探究对该反应速率的影响。
③实验a和探究大理石颗粒大小对该反应速率的影响。
④根据表格中的数据写出2个与实验目的相对应的实验结论:
(查阅资料)
Ⅰ.过氧化钠是一种淡黄色固体,常用在呼吸面具和潜艇中制造氧气。其原理是:2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
Ⅱ.常温常压下,O2和CO2的密度分别为1.3g/L、1.8g/L。
(分析猜想)
Ⅰ.只有Na2O2;Ⅱ.含有Na2O2和Na2CO3两种物质;
Ⅲ.含有两种物质;Ⅳ.含有。
首先按如图连接好装置。用电子秤称取 1.00g 固体样品置于干燥的仪器 X 中,向分液漏斗中加入一定量的蒸馏水。

仪器X的名称是。打开分液漏斗活塞,将蒸馏水加入仪器X中。反应完全后(无固体剩余),注射器内收集到80.0mL气体,说明样品中含有g Na2O2(计算结果保留到小数点后两位)。
通过以上实验操作得出结论,猜想是正确的(填序号)。