 对玻璃片哈气
B .
对玻璃片哈气
B .  切割玻璃
C .
切割玻璃
C .  菜刀生锈
D .
菜刀生锈
D .  橙子榨汁
橙子榨汁



| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 2 | 30 | 20 | 10 |
| 反应后的质量/g | m | 39 | 5 | 16 |

 B .
B . 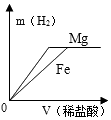 C .
C .  D .
D . 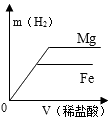

①如图所标物质中属于金属材料的是。(填一种即可)
②车架表面刷油漆主要是为了防锈,其原理是。

已知:①Fe与Fe2(SO4)3溶液能发生反应生成FeSO4②溶液B中只有一种溶质。

查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑(产物NaAlO2溶于水);Mg、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除Al外,还含有Mg。
猜想2:该合金粉末中除Al外,还含有Cu。
猜想3:该合金粉末中除Al外,还含有(填化学式)。
|
实验方案 |
实现现象 |
结论 |
|
①取一定量的硬铝粉末,加过量的 ,充分反应后过滤,滤渣备用。 |
粉末部分溶解,并有气体放出。 |
硬铝中一定含有 。 |
|
②取步骤①所得滤渣,加过量的 ,充分反应。 |
滤渣部分溶解,并有气体放出。 |
硬铝中一定含有 。 |
方案一:;
方案二:。
(提出问题)脱氧剂的成分是什么?
甲同学:可能有铁粉
乙同学:可能有炭粉,因为活性炭具有性,可以将空气中的氧气富集在脱氧剂周围。
|
实验步骤 |
实验现象 |
实验结论 |
|
向脱氧剂中加入足量的 |
固体部分溶解,有气泡产生 |
甲、乙同学的猜想均成立 |
|
过滤,将滤渣与氧化铜混合加热 |
|
滤渣与氧化铜的反应需在高温条件下进行,从实验装置角度考虑,可以通过的方法来提供高温。

②硅藻土高于或低于最佳量时,脱氧速度会减慢。请分别分析可能的原因,。
③脱氧剂的脱氧速度还有可能受哪些因素影响?请写出一条并说明理由:。