 B . 分离岀AgNO3溶液中的AgCl
B . 分离岀AgNO3溶液中的AgCl 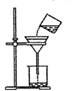 C . 检查装置气密性
C . 检查装置气密性 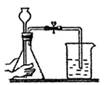 D . 收集氧气
D . 收集氧气 
| 选项 | 实验目的 | 实验设计 |
| A | 除去食盐中少量的硫酸钠 | 溶解,过滤 |
| B | 探究铜、锌的金属活动性 | 将打磨好的铜片、锌片分别插入稀硫酸中 |
| C | 探究稀盐酸和NaOH溶液是否完全反应 | 向反应后溶液中加入AgNO3溶液 |
| D | 证明一块岩石的主要成分是碳酸盐 | 取样,滴加盐酸溶液,观察现象 |

 B . 向一定量的锌粒中不断加入稀硫酸直至过量
B . 向一定量的锌粒中不断加入稀硫酸直至过量  C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉  D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液
D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液 




①水和氢氧化钠;②稀硫酸和锌;③稀盐酸和石灰石:
④硝酸银溶液和氯化钠固体;⑤水和消石灰;⑥稀盐酸和银


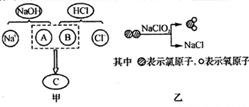
A.Fe B.酚酞溶液 C.CuSO4 D.Ba(NO3)2




①若只观察到有气泡产生的现象,则试管A的溶液中含有的阴离子是 (填符号)。
②若开始阶段观察到有气泡,一段时间后又出现白色沉淀的现象。待反应结束后,将烧杯中混合液过滤,滤液中的溶质除氯化钾外,还可能有 (填化学式)。

①组装仪器,并检查装置的气密性
②在仪器中加入药品,其中粗锌的质量为m1;
③用电子天平称量出整套装置(含药品)的总质量为m2;
④关闭a处止水夹、打开b处止水夹,然后打开分液漏斗的活塞,向锥形瓶中注入全部的稀硫酸(足量),随即关闭分液漏斗的活塞;
⑤充分反应后,打开a处止水夹,向装置中持续缓慢地鼓入空气,将产生的氢气从装置中排出;
⑥第二次称量整套装置(含反应后物质)的质量为m3。




|
序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
质量 |
2m |
m |
m/2 |
m/3 |
m/4 |
m/5 |
m/6 |

①该化工厂排放的污水中主要成分是盐酸、提取未处理的污水水样,测得pH=3;
②处理污水步骤之一是:污水进入中和池进行中和处理,所用的材料是较经济的熟石灰;
③提取经过处理后可以排放的水样,测得pH在7左右。
根据上述提供的资料,回答下列问题

“锡纸”在中间狭窄的地方先开始燃烧的原因是:由于电源短路,产生较大的电流,且“锡纸”在中间狭窄的地方电阻 (填大或小),产生的热量多,温度先达到。电池在工作时将 能转化为电能。
查阅资料:“锡纸”是锡箔或铝箔和纸粘合而成。
实验探究:取包口香糖的“锡纸”,将有金属的一面打磨后,朝上放在点滴板上;并向其表面滴加氯化锌溶液,观察到有深灰色固体析出。
实验分析:
①通过上述实验现象,可知“锡纸”是(选填“锡”或“铝”)箔和纸粘合而成;
②实验中打磨“锡纸”的目的是 ;
③下列物质的溶液可以替代氯化锌溶液完成上述探究实验的是 (选填字母)
A.硝酸银 B.稀盐酸 C.硫酸亚铁 D.氯化镁