①1s22s22p3 ②1s22s22p63s23p3③1s22s22p5 ④1s22s22p63s23p2
①不和碘或水起化学反应 ②能溶于水 ③不溶于水 ④应是极性溶剂 ⑤应是非极性溶剂.
①金刚石 ②晶体硅 ③碳化硅
①互为手性异构体的分子互为镜像
②利用手性催化剂合成可得到一种或主要得到一种手性分子
③手性异构体分子组成相同
④手性异构体性质相同
你认为正确的是( )
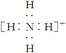 ,离子呈平面正方形结构
D . NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
,离子呈平面正方形结构
D . NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
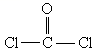 ,COCl2分子内含有( )
,COCl2分子内含有( )
①HF的熔、沸点比ⅦA族其他元素氢化物的高 ②乙醇可以与水以任意比互溶 ③冰的密度比液态水的密度小 ④水分子高温下也很稳定 ⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
①此元素原子的电子总数是;
②有个能层,个能级;
③它的电子排布式为。
①S;②Ca2+;③Cl-;④Ni2+;⑤Ge;⑥Mn2+。
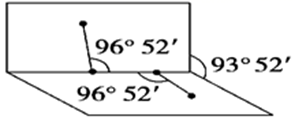
H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答: