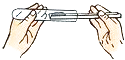
 加土壤颗粒
B .
加土壤颗粒
B . 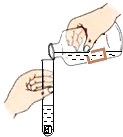 加水溶解
C .
加水溶解
C . 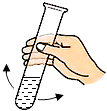 振荡试管
D .
振荡试管
D . 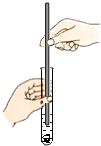 用玻璃棒蘸取清液
用玻璃棒蘸取清液
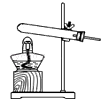 B .
B . 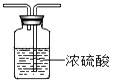 C .
C . 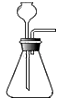 D .
D . 选项 | 性质 | 用途 |
A | 氧气具有助燃性 | 用于火箭发射 |
B | 浓硫酸具有腐蚀性 | 干燥氢气 |
C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
D | 氢氧化钠能与某些非金属氧化物反应 | 吸收二氧化硫 |
选项 | 实验目的 | 实验操作 |
A | 检验NaCl中含有Na2CO3 | 加水溶解 |
B | 鉴别NaOH和Ca(OH)2溶液 | 加Na2CO3溶液 |
C | 除去FeSO4溶液中的CuSO4 | 加适量Zn粉,过滤 |
D | 除去CO2中的CO | 通过足量NaOH溶液 |
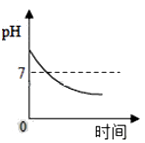 服用胃舒平[主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
B .
服用胃舒平[主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
B . 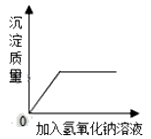 向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液
C .
向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液
C . 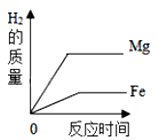 将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
D .
将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
D . 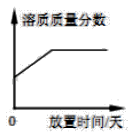 浓盐酸敞口放置
浓盐酸敞口放置
①稀盐酸 ②消石灰 ③碳酸钙 ④氢氧化钠 ⑤氢气 ⑥硝酸钾
如图2折叠纸的情形中错误的是(填字母序号);
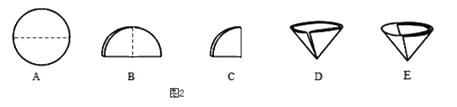
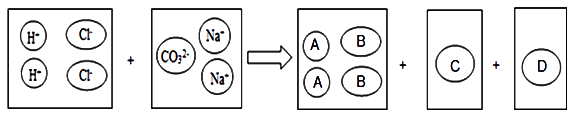
我们现阶段所学的复分解反应的实质是反应物中的一些阴、阳离子相互结合生成水、气体或沉淀,如BaCl2溶液和Na2SO4溶液反应,实际参加反应的是Ba2+和SO42﹣结合生成BaSO4沉淀,而Cl﹣和Na+则是“旁观者”,并没有参加反应,仍然在溶液中。请在下图圆圈A、B、C、D填入适当的分子或离子符号,体现稀盐酸和碳酸钠溶液反应的实质:
稀硫酸 | 氢氧化钙溶液 | |
实验现象 | 溶液变蓝色 |
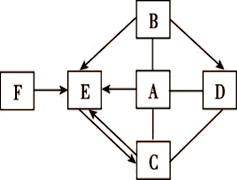
如图所示A~F是初中化学常见的物质。图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出)。其中A是人体胃液中含有的酸,A和B发生中和反应可得到生活中常用的一种调味品,固体C常用于改良酸性土壤。
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师请各小组同学开展探究。

【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里。
由此猜测:这瓶无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液。
甲同学根据标签上的组成元素认为一定不可能是溶液。
乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是。
实验操作 | 实验现象 |
①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液。 ②静置、过滤,向白色沉淀中滴加。 | 产生白色沉淀。 产生大量气泡,沉淀消失。 |
该瓶无色溶液的溶质是,生成白色沉淀的化学方程式是。
丙同学认为原设计的实验还可简化,同样达到鉴别的目的。丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
实验操作 | 实验现象 |
取少量该无色溶液于试管中,。 | 。 |
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是,理由是.
【实验探究】
①丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有.
②为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生白色沉淀 | |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出②中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①实验操作中的错误是.
②实验方案中也有一个是错误的,错误的原因是.