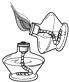
 点燃酒精灯
B .
点燃酒精灯
B .  加热液体
D .
加热液体
D . 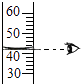 读取液体体积
读取液体体积
A.化学与安全 | B.化学与材料 |
重金属中毒﹣可喝鲜牛奶 解毒 煤气泄漏﹣应关闭气阀、开窗通风 | 水泥、玻璃﹣都是无机材料 玻璃钢、铝合金﹣都是金属材料 |
C.化学与食品 | D.化学与健康 |
蛋白质、淀粉﹣用碘酒可鉴别 糖类、油脂﹣组成元素相同 | 缺锌﹣易得侏儒症 缺铁﹣易得贫血症 |

物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 | |
A | CO2 | CO | O2 | 点燃 |
B | KCl | MnO2 | 水 | 充分溶解、过滤、蒸发 |
C | NaCl | Na2CO3 | 硝酸 | 足量加入硝酸溶液 |
D | Cu(NO3)2溶液 | AgNO3 | Cu粉 | 加入过量的铜粉,过滤 |

①氨气分子;②碳酸钙中阴离子;③过氧化氢中氧元素的化合价;④侯氏联合制碱法中的“碱”是_;⑤最简单的有机物是;
⑥食品袋中的“双吸剂”
①湿法冶铜:;反应类型;
②高炉炼铁的原理:;
③实验室用氯酸钾制取氧气的反应:.
量的CO2 , 要提高100mL水中CO2的溶解量,可、(写两种方法即可).要证明盐汽水中含CO2 , 可用的方法检验CO2的
存在.
已知过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂,利用人呼出的二氧化碳与Na2O2反应放出O2 , 供给人的正常生命活动,该反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2 . 某同学利用该反应原理制取氧气,设计了如图一所示的实验装置. 
A.排水集气法 B.向下排空气法 C.向上排空气法 D.真空袋收集法
碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业.有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如图所示.

已知:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应.但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度.
|
温度/℃ |
0 |
40 |
80 |
|
Ca(OH)2溶解度/g |
0.187 |
0.141 |
0.094 |
|
Ba(OH)2溶解度/g |
1.67 |
8.22 |
101.4 |
A.降温,过滤;B.加热,过滤
氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物.
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气.
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气.
【氢化钙的制备】
氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气.氢化钙通常用氢气与金属钙加热制取,图1是模拟制取装置:

①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
①写出CaH2与水反应的化学方程式
②该同学的判断不正确,原因是
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计).样品纯度的测定步骤如下:
①检查装置气密性,方法为
②装入药品,按图2(固定装置省略)所示连接仪器.
③调整水准管高度,使量气装置两边的液面保持同一水平.读取液面所在的刻度数据为10.0mL.
④将Y型管中水与氢化钙样品混合,操作为
⑤反应结束,冷却至室温,再次,读取液面所在刻度数据为110.0mL.
①如何判断样品与水完全反应:
②反应生成氢气的体积为mL.
③已知该实验条件下,氢气的密度为0.09mg/mL.样品中氢化钙的纯度为.(结果精确到0.1%)
①Y型管中残留有氢气,对测定结果的影响是.
②未冷却至室温即读数,对测定结果的影响是.