


| 选项 | 实验操作和现象 | 结论 |
| A | 向盛有KI3溶液的试管中加入适量CCl4 , 振荡后静置,CCl4层显紫色(已知I3- | KI3在CCl4中的溶解度比在水中的大 |
| B | 向淀粉溶液中加入稀硫酸水浴加热后,再加入银氨溶液水浴加热,未出现银镜 | 淀粉未发生水解 |
| C | 向饱和Na2CO3溶液中加入少量BaSO4粉末搅拌,过滤,向洗净的沉淀中加入稀盐酸,有气体放出 | Ksp(BaSO4)>Ksp(BaCO3) |
| D | 向新制饱和氯水中滴加紫色石蕊试液,溶液先变红后褪色 | 氯水具有酸性和漂白性 |


已知:25 ℃时,Ksp(CaF2)=1.5×10-10、Ksp(MgF2)=7.5×10-11。
①除铁铝时,在搅拌条件下先加入H2O2溶液,再加入NaOH溶液调节pH。加入H2O2溶液时发生反应的离子方程式为。
②除钙镁步骤中,当Ca2+、Mg2+沉淀完全时,溶液中 =。

①沉锰过程发生反应的离子方程式为。该过程中加入适当过量的NH4HCO3的原因是。
②当温度超过30 ℃,沉锰反应的锰沉淀率随温度升高而下降的原因是。
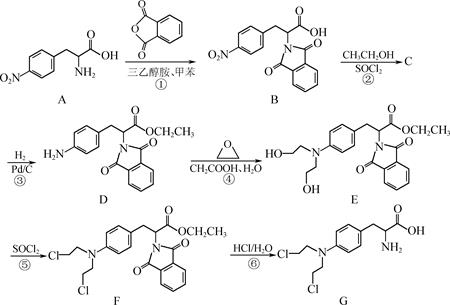
①含有苯环,且苯环上有3个取代基;② 分子中含有2个手性碳原子;③ 能发生水解反应,水解产物之一是α氨基酸,另一水解产物分子中只有3种不同化学环境的氢。
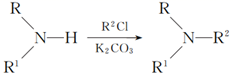 (R、R1代表烃基或H,R2代表烃基)。写出以
(R、R1代表烃基或H,R2代表烃基)。写出以 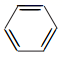 和
和  )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
步骤1:CuSO4标准液的配制与标定。取一定量胆矾溶于水,加入适量稀H2SO4 , 转移到1 L容量瓶中定容。准确量取25.00 mL所配溶液置于250 mL锥形瓶中,用0.005 0 mol·L-1EDTA标准液滴定至终点。重复3次实验,平均消耗EDTA标准液10.00 mL 。
步骤2:样品分析。取10.00 mL矿业废水置于250 mL锥形瓶中,加入一定体积柠檬酸,煮沸;再加入0.005 0 mol·L-1的EDTA标准液20.00 mL,调节溶液pH至4.0,加热;冷却后用CuSO4标准液滴定至终点,消耗CuSO4标准液30.00 mL。(已知:Cu2+、Al3+与EDTA反应的化学计量比均为1∶1)
步骤1中,重复3次实验的目的是。
② Fe3+也可与EDTA反应,步骤2中加入的柠檬酸是作为掩蔽剂,消除Fe3+的干扰。若该矿业废水样品中含有Fe3+ , 而上述实验中未加入柠檬酸,则测定的Al3+含量将(填“偏大”“偏小”或“无影响”)。
③计算该矿业废水中Al3+的含量(用mg·L-1表示)(写出计算过程)。

已知:① 2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O;
② 2ClO2+2NaOH=NaClO2+NaClO3+H2O;
③温度高于60 ℃时,NaClO2发生分解生成NaClO3和NaCl。
①研究表明,实验时吸收液中H2O2与NaOH的物料比需要控制在0.8左右,原因可能是。
②在吸收液中H2O2和NaOH的物料比、浓度和体积不变的条件下,控制反应在0~3 ℃进行,实验中可采取的措施是。
③装置Ⅱ的作用是。

![]() +(CH3CO)2O
+(CH3CO)2O
![]() +CH3COOH
+CH3COOH
过程中发生的副反应如下:

实验步骤如下:
步骤1:在三颈烧瓶中加入3 mL苯甲醛、8 mL乙酸酐和4.2 g K2CO3固体,搅拌,控制温度在150~170 ℃,加热回流45 min。
步骤2:向反应液中分批加入20 mL水,再加入Na2CO3固体调节溶液pH至8,然后进行水蒸气蒸馏。(装置如图)

步骤3:待三颈烧瓶中的剩余液体冷却后,加入活性炭,煮沸10~15 min,趁热过滤。
步骤4:将滤液冷却至室温,用盐酸酸化,待晶体析出完全后进行抽滤,用冷水洗涤晶体,干燥得到产品。
①以木屑和FeCl3·6H2O为原料,在N2氛围中迅速升温至600 ℃,保持2 h,过程中木屑先转化为木炭,最终制得木炭包覆纳米零价铁。制备木炭包覆纳米零价铁过程中,木炭的作用有吸附和。
②木炭包覆纳米零价铁在碱性废水中形成许多微电池,加速SeO32-的还原过程。SeO32-在微电池正极上转化为单质Se,其电极反应式为。
①结构态的绿锈具有优异的吸附性能,而且游离态的Fe3+还易水解生成Fe(OH)3胶体进一步吸附SeO32-。写出Fe3+水解的离子方程式:。
②不同FeⅡ/FeⅢ组成的绿锈对SeO32-去除效果的影响结果如图1所示。随着绿锈组成中FeⅡ/FeⅢ比值的增大,绿锈的除硒效果先减小后增大的原因可能是。

③废水的初始pH会对绿锈去除SeO32-的效果产生影响,关系如图2所示。当初始pH增大至11时,SeO32-的去除效果突然迅速减小的原因是。