|
温度 |
10℃ |
20℃ |
|
NaHCO3的溶解度(g/100g水) |
8.1 |
9.6 |
|
Ca(HCO3)2的溶解度(g/100g水) |
16.6 |
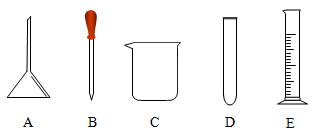
回答下列问题:
|
离子 |
K+ |
Ca2+ |
Mg2+ |
HCO | Cl- |
| 含量(mg/L) | 310 | 491 | 129 | 470 | 26.1 |
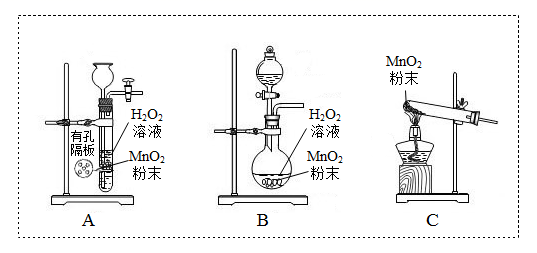
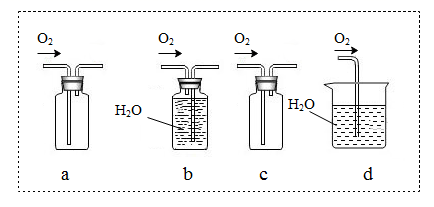
①H2O2显酸性消耗了NaOH,而使红色褪去;
②H2O2分解产生的氧原子与酚酞反应破坏其结构,而使红色褪去。究竟哪种猜想合理?请用本次实验用过的试剂设计实验(补充完实验方案)。有兴趣的同学可在后续学习中通过实验得出结论。
已知:物质沉淀的pH见下表:
|
物质 |
Mg(OH)2 |
Fe(OH)3 |
|
开始沉淀的pH |
8.9 |
1.5 |
|
完全沉淀的pH |
10.9 |
2.8 |
①菱铁矿中镁元素的质量分数为(不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。