 B . CaCl2的电子式为:
B . CaCl2的电子式为: 
 B .
B .  C .
C .  D .
D . 
| A | B | C | D |
| | | | |
| 普通干电池 | 对讲机镍镉电池 | 汽车铅蓄电池 | 手机锂离子电池 |
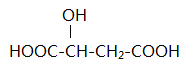 ,下列说法正确的是( )
,下列说法正确的是( )
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ |
Ⅵ |
Ⅶ |
0 |
|
|
1 |
① |
② |
||||||
|
2 |
③ |
④ |
⑤ |
⑥ |
||||
|
3 |
⑦ |
⑧ |
⑨ |
⑩ |


①A→B:,反应。
②苯→硝基苯:,反应。

主要步骤如下:
a.配制一定比例的浓硫酸与浓硝酸混合酸,加入反应器中
b.在50~60℃下发生反应,直至反应结束
c.将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯
d.向室温下的混合酸中逐滴加入一定质量的苯,充分振荡,混合均匀
e.除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤
回答下列问题:
①实验操作的正确顺序是(填字母)。
②步骤b中的加热方法为,步骤e中洗涤和分高粗硝基苯应使用的主要仪器是,粗产品用5%NaOH溶液洗涤的目的是