①石英的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③太阳能电池的主要成分是硅,太阳能电池在生活中的应用有利于环保、节能
④二氧化硅的熔点高,硬度大,所以可用来制造电子部件和光学器件
⑤水玻璃中含有三种元素,主要用来制备硅胶和木材防火剂

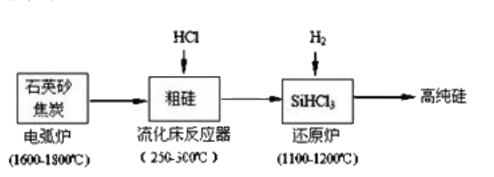
SiHCl3极易水解且生成某种可燃性气体,其完全水解的产物为_。
|
物质 |
Si |
SiCl4 |
SiHCl3 |
SiH2Cl2 |
SiH3Cl |
HCl |
SiH4 |
|
熔点/℃ |
1410 |
-70.4 |
-126.5 |
-122 |
-118 |
-114.2 |
-185 |
|
沸点/℃ |
2355 |
57.6 |
31.8 |
8.2 |
-30.4 |
-84.9 |
-111.9 |
属于电解质的有。
偏铝酸钠溶液中通入足量二氧化碳反应的离子方程式为:。
![]()
写出步骤①的化学方程式。
步骤②的产物经过冷凝后得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃),提纯SiHCl3主要操作的名称是。
 (少量)
(少量)