 C . 易拉罐
C . 易拉罐  D . 垃圾袋
D . 垃圾袋 
 B . 干燥氧气
B . 干燥氧气  C . 闻气体的气味
C . 闻气体的气味  D . 测定溶液的pH
D . 测定溶液的pH 
|
选项 |
酸 |
碱 |
盐 |
氧化物 |
|
A |
HNO3 |
Na2CO3 |
Cu(NO3)2 |
Fe3O4 |
|
B |
HCl |
NaOH |
NaCl |
C2H6O |
|
C |
H2SO4 |
KOH |
NH4NO3 |
H2O |
|
D |
H2O2 |
Ca(OH)2 |
ZnSO4 |
O2 |

| 选项 | 物质 | 所含杂质 | 出去杂质的方法 |
| A | H2 | 少量水蒸气 | 通过浓硫酸 |
| B | SO2 | 少量HCl | 通入足量的NaOH溶液,干燥 |
| C | NaCl溶液 | 少量的CaCl2 | 加入适量Na2CO3溶液, 过滤 |
| D | FeCl2溶液 | 少量的CuCl2 | 加入足量的铁屑充分反应后,过滤 |


![]()



【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O==2NaOH+H2↑
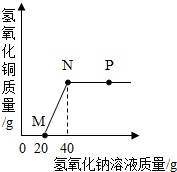
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示
|
实验编号 |
钠块大小 |
硫酸铜溶液 |
实验中产生沉淀的现象 |
|
① |
绿豆大小 |
稀溶液10mL |
产生蓝绿色沉淀 |
|
② |
绿豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀 |
|
③ |
豌豆大小 |
稀溶液10mL |
产生蓝色絮状沉淀 |
|
④ |
豌豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
a.上述实验中均未观察到色固体生成,由此判断猜想一错误。
b.实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误。
a.实验中生成氢氧化铜沉淀的原理是。
b.由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有。
c.为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热。
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热。
请从两个方案中选出合理的方案,并说明理由。



|
表:H2S回收工艺的各项生产成本 |
|
|
项目 |
单价(元/吨) |
|
NaOH |
2500 |
|
Na2S |
5000 |
|
辅助费用(以处理1吨H2S计) |
1000 |


|
|
反应前 |
反应后 |
|
实验数据 |
氯酸钾和二氧化锰的总质量 |
剩余固体混合物的总质量 |
|
80g |
55g |

为探究反应结束之后氯酸钾是否完全分解,该兴趣小组的同学将反应后的混合物放在烧杯中加水充分溶解、过滤、烘干、得到不溶于水的固体物质15g。(不考虑实验过程中物质的损失)