 熄灭酒精灯
B .
熄灭酒精灯
B .  塞紧橡胶塞
C .
塞紧橡胶塞
C .  移走加热后的蒸发皿
D .
移走加热后的蒸发皿
D .  加热液体
加热液体
| A.有关原子的描述 | B.实验现象 |
| ①某原子的相对原子质量,是该原子的质量与C-12原子质量的1/12作比,得到的结果 ②原子都由质子、中子、电子构成 | ①硫在氧气中燃烧,产生明亮的蓝紫色火焰,生成刺激性气味气体 ②二氧化碳气体通入紫色石蕊试液,再加热溶液,溶液颜色变化为紫色→红色→紫色 |
| C.实验推论 | D.实验操作 |
| ①过滤能去除水中的一些杂质,所以过滤能去除食盐水中的氯化钠 ②加热高锰酸钾制取氧气时,水槽中的水变红了,可能是因为试管口没有放一小团棉花 | ①部分实验的操作顺序:先检查气密性,再装药品 ②排水法收集氧气后,先盖好玻璃片再倒放桌上 |
 B .
B . 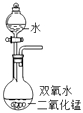 C .
C . 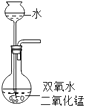 D .
D . 
 B .
B .  C .
C .  D .
D . 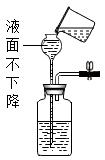


 B . 并列关系
B . 并列关系  C . 包含关系
C . 包含关系  D . 交叉关系
D . 交叉关系 
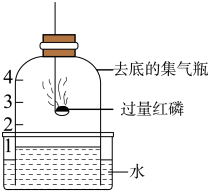

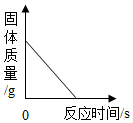 加热一定质量的碳酸氢铵固体
B .
加热一定质量的碳酸氢铵固体
B . 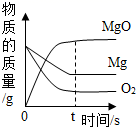 镁在氧气中燃烧
C .
镁在氧气中燃烧
C . 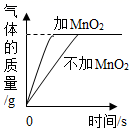 等质量、等浓度的双氧水完全分解
D .
等质量、等浓度的双氧水完全分解
D .  加热一定质量的高锰酸钾固体
加热一定质量的高锰酸钾固体

①铕元素属于元素(填“金属”或“非金属"),铕原子中的质子数是。
②图中152.0表示的是铕元素的。
③氯化铕中铕元素的化合价为,相应价态下氧化物的化学式为,该氧化物的相对分子质量为。
①从宏观角度看,图中三种物质的组成中都含有(填“氧原子”或“氧元素”),从微观角度看,图中三种物质都是由(填“分子”、“原子”或“离子”)构成的;
②写出图中实现b转化的化学反应符号表达式:。
①由图可知,氯和溴具有相似化学性质的原因是。
②画出氯离子的结构示意图。
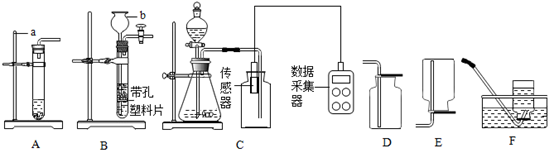
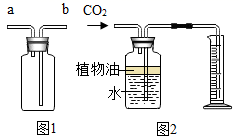
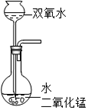
②若用上图2所示装置来测量生成的CO2的体积,其中在水面上放一层植物油的目的是,植物油上方原有的空气对实验结果(填“有”或“无”)明显影响。
③已知氨气的密度比空气小,极易溶于水,则收集氨气应选择的装置是(选填装置编号D或E或F)
|
CO2的体积分数/% |
34.4 |
36.3 |
39.2 |
43.1 |
44.3 |
48.8 |
51.5 |
|
木条的燃烧状况 |
不灭 |
不灭 |
火焰变小 |
火焰变小 |
熄灭 |
熄灭 |
熄灭 |
当瓶内O2的体积分数为12%时,放在瓶口的木条(填“不灭”“火焰变小”或“熄灭”)(不考虑空气中原有CO2以及实验产生的水蒸气对计算结果的影响);请写出计算过程。
a用容积较小的锥形瓶
b减慢滴加液体的速度
c加热反应物
d降低液体反应物的浓度
(提出问题)氧化铜能否作过氧化氢溶液分解的催化剂?如果能,其催化效果是否比二氧化锰好呢?
(实验探究)
|
实验步骤 |
实验现象 |
|
Ⅰ.分别量取5mL 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入1g氧化铜粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 |
A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
|
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 |
试管中均产生气泡,带火星木条均复燃 |
|
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量为ag |
|
|
Ⅳ.分别量取5mL 5%过氧化氢溶液放入C、D两支试管中,向C试管中加入1g氧化铜粉末,向D试管中加入bg二氧化锰粉末,观察现象。 |
(实验结论)
实验设计IV的目的是,其中b=g。
查阅资料得知,氧化铁、硫酸铜、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是。
a二氧化锰不只是过氧化氢溶液分解的催化剂
b同一个化学反应可以有多种催化剂
c催化剂提高了工业生产能力
d用作催化剂的物质不可能是其他反应的反应物或生成物
a科学使用高效低毒的农药、化肥
b大力发展虾蟹养殖
c生活污水先净化后再排放
d工厂废水经处理达标后再排放