 加多宝凉茶
B .
加多宝凉茶
B .  蒙牛酸奶
C .
蒙牛酸奶
C .  屈臣氏蒸馏水
屈臣氏蒸馏水
 B .
B .  C .
C .  D .
D . 


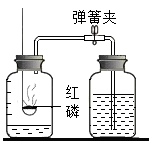 测定空气里氧气的含量
B .
测定空气里氧气的含量
B . 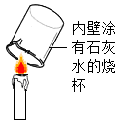 验证蜡烛含有碳元素
C .
验证蜡烛含有碳元素
C . 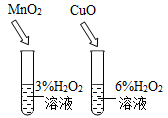 比较不同催化剂的催化效果
D .
比较不同催化剂的催化效果
D . 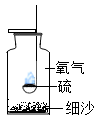 硫在氧气中燃烧
硫在氧气中燃烧
 B . 表示加热高锰酸钾制氧气剩余固体质量与时间的关系
B . 表示加热高锰酸钾制氧气剩余固体质量与时间的关系  C . 表示空气中氮气和氧气相对含量
C . 表示空气中氮气和氧气相对含量  D . 表示吸收极易溶于水的气体,且防止产生倒吸现象
D . 表示吸收极易溶于水的气体,且防止产生倒吸现象 

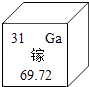
①用 ![]() ”可表示的微粒是 (填化学符号)。
”可表示的微粒是 (填化学符号)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图 3 可表示空气微观模型的是 (填字母)。

①氖气
②步骤②的反应中没有改变的微粒是
③铵根离子
④标出 NH3中氮元素的化合价
⑤步骤②反应的化学方程式是。
⑥步骤③反应的化学方程式是。
①从标签上看碳酸氢铵具有的化学性质是 (填字母)。
A 易溶于水B 有挥发性C 受热易分解
②该袋化肥中氮元素的质量至少为kg。
③若杂质中不含氮元素,图 2 所示的化肥中碳酸氢铵的质量分数为(计算结果精确到 0.1%)。

电解一段时间后,将两极产生的气体的体积与时间的关系绘制成图②所示的平面直角坐标系,回答:
① 由图①、②看出,A 气体是(填化学式),B 气体在电源的极。
② 0~8min A、B 气体的体积比为。
A 水的电解 B 水的蒸馏 C 氢气在氧气中燃烧 D 水的煮沸
已知:①相同条件下,气体的体积比等于气体的分子个数比;
②常温常压时,1L 水可溶解 0.031L O2、0.57L O3。
A 水在通电时能发生分解反应
B 实验中若加入少量NaOH 溶液,则导电性增强
C 从实验结果可以确定,相同条件下,H2在水中的溶解度比O2的小
D 若右侧试管内产生少量 O3 , 也会使左右两侧试管内气体体积比略大于 2:1
下列是有关水的性质、变化和用途的描述:
A 通常为无色、无味的液体B 水是常用的灭火剂
C 氢气在氧气中能燃烧生成水D 水能与氧化钙反应生成氢氧化钙。
①其中属于水的化学性质的是(填字母)。
②写出D 中反应的化学方程式。

图 1 是利用气压传感器测定红磷燃烧时集气瓶内气压变化的实验装置。图 2 是集气瓶内气压的变化情况。图 3 是利用铜粉与氧气加热后反应生成氧化铜的原理,测定空气中氧气含量的实验装置。
A BC 段气压增大的主要原因是燃烧放热
B CD 段气压减小的主要原因是集气瓶内氧气不断被消耗且瓶内温度逐渐冷却
C DE 段气压增大的主要原因是烧杯中的水进入集气瓶
D 若用木炭代替红磷完成此实验,集气瓶内气压变化趋势与图 2 基本一致
①组装装置,检查装置的气密性;
②向试管中加入足量的铜粉,铜粉要足量的原因是;
③点燃酒精灯,不停地抽拉注射器的活塞,充分反应后停止加热。试管中发生的化学方程式为。实验前,该注射器中空气的体积至少为mL,才能顺利的完成实验。
反思:探究小组通过图 3 实验测定出的结果始终不准确,通过分析改良后,认为图 4 实验更合理,图 4 实验合理的理由是,若实验过程中用酒精灯在铜粉部位加热时,没有不断推拉注射器,则可能导致测定的空气中氧气的体积分数(填“偏大”、“偏小”、“不变”)。


写出图中标号仪器的名称:①;②。


①甲中浸有紫色石蕊溶液的纸花变红,使其变红的物质是。(填化学式)
②乙中的现象是,该反应的化学方程式为。
③丙中蜡烛由下而上依次熄灭,此现象证明二氧化碳的化学性质是,物理性质是二氧化碳的密度比空气(填“大”或“小”)。
〖探究 1〗用氯酸钾、二氧化锰为原料制取并收集氧气
该方法制取氧气的化学方程式为;能用排水法收集 氧气是因为氧气;


①向锥形瓶中加入一定量的二氧化锰,注射器中吸入 20mLH2O2溶液。
②将注射器中的 H2O2溶液平均分 4 次推入锥形瓶中:每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
| 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 | |
| 收集气体的总体积/mL | 60 | 120 | x | y |
表中的数据 x=,根据表中的数据可以推测 20mLH2O2溶液总共产生 O2的体积为mL。