 B .
B .  C .
C .  D .
D . 
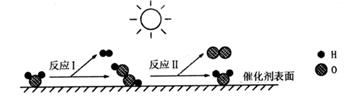
![]()

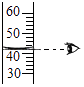 量取液体读数
B .
量取液体读数
B . 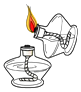 引燃酒精灯
C .
引燃酒精灯
C . 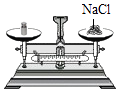 称量固体
D .
称量固体
D . 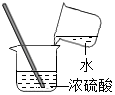 稀释浓硫酸
稀释浓硫酸
 B . 观察乳化现象
B . 观察乳化现象  C . 观察铁锈蚀的现象
C . 观察铁锈蚀的现象  D . 验证面粉在一定条件下能爆炸
D . 验证面粉在一定条件下能爆炸 
| 选项 | 物质 | 少量杂质 | 所用试剂和操作方法 |
| A | H2O | NaCl | 向水中加入活性炭吸附 |
| B | 铜粉 | CuO | 在空气中充分灼烧 |
| C | N2 | 水蒸气 | 通过足量的氢氧化钠固体干燥剂 |
| D | Na0H | Na2CO3 | 加适量的稀盐酸 |
| A.性质与用途 | ①氧气具有可燃性,可用于炼钢②干冰升华时能吸收大量的热,可作制冷剂 | B.物质与分类 | ①烧碱、纯碱都属于碱②二氧化锰、氧化铝属于氧化物 |
| C.化学与资源 | ①可燃冰将成为未来新能源②地球上的水储量丰富,但可供利用的淡水资源有限 | D.化学与生活 | ①碳酸氢钠可用于治疗胃酸过多症②厨房燃气泄漏应立即打开排气扇通风换气 |
 B .
B .  C .
C .  D .
D . 

①Na属于(填“金属”或“非金属”)元素,其原子的核电荷数为。
②Mg原子的结构示意图为  ,则镁离子的核外电子数为。
,则镁离子的核外电子数为。
③周期表中氯元素的有关信息如右图所示,图中“35.45”所表示的含义是。
![]()
④由镁和氯构成的盐的化学式为 。

①写出物质X的化学式:。
②写出由物质Y转化为CuSO4的化学反应方程式: 。

②“高炉气体”中的(填化学式)会导致酸雨。
③炉渣的主要成分是CaSiO3 , 其中硅元素的化合价为 。
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红棕色
C.b处可用澄清石灰水检验生成的CO2
D.可用Na0H溶液吸收尾气中的CO
②用化学方程式表示利用CO炼铁的原理。
|
气体 |
方法(或原理) |
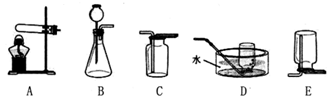
发生装置 |
收集装置 |
|
O2 |
方法1:加热混有二氧化锰的氯酸钾固体。反应中二氧化锰所起的作用是。 |
均可选择A装置(可根据需要添加棉花) |
均可选择装置(填标号) |
|
方法2:加热(填化学式) |
|||
|
方法3:分解过氧化氢溶液,化学方程式为。 |
均可选择装置(填标号) |
||
|
CO2 |
用稀盐酸和大理石反应来制取 |
|
方案 |
现象 |
结论 |
|
方案1:将带火星的木条分别伸入两个集气瓶中 |
若带火星的木条 |
则该瓶气体是O2 |
|
方案2:向两个集气瓶中分别滴入少量的溶液,振荡 |
若溶液变浑浊 |
则该瓶气体是CO2 |
|
方案3:向两个集气瓶中分别倒入少量的水,振荡后再滴加几滴紫色石蕊溶液 |
若紫色石蕊溶液变为色 |
则该瓶气体是CO2 |
|
…… |
…… |
…… |
甲、a→b→c
乙、b→a→c
丙、c→a→b
[猜想假设]猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和
猜想四:NaOH、Na2CO3和Ca(OH)2
[讨论分析]经过讨论认为最不合理的是猜想,原因是。
|
实验步骤 |
现象 |
结论 |
|
步骤Ⅰ:取少量滤液,向其中加入足量盐酸 |
|
猜想二不成立 |
|
步骤Ⅱ:另取少量滤液,向其中滴入适量Na2CO3溶液现象 |
产生白色沉淀 |
猜想成立 |
![]()
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
①结合图表分析,趁热过滤的原因是 。
②操作a的名称是。
③滤液2的溶质是。

①B物质是。
②反应i能发生的原因是。
③反应i的化学方程式是,该反应所属的基本反应类型是。
④若只用一步操作实现反应ii,能否加入氯化钾?(填“能” 或“不能”)。说明理由:。
