 B .
B .  C .
C .  D .
D . 
 冰雪融化
B .
冰雪融化
B .  水果榨汁
C .
水果榨汁
C .  分离液态空气
D .
分离液态空气
D .  葡萄酿酒
葡萄酿酒
 检查装置的气密性
B .
检查装置的气密性
B .  二氧化碳验满
C .
二氧化碳验满
C .  取用粉末状药品
D .
取用粉末状药品
D .  给液体物质加热
给液体物质加热

 中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B .
中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B .  中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C .
中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C .  中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D .
中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D .  中镁条剧烈燃烧的现象可知,燃烧不一定需要氧气
中镁条剧烈燃烧的现象可知,燃烧不一定需要氧气
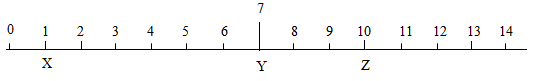

 表示向一定量的稀硫酸中加入足量的锌粒
B .
表示向一定量的稀硫酸中加入足量的锌粒
B .  表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液
C .
表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液
C .  表示向一定量的氢氧化钠溶液中滴加稀硫酸至恰好完全反应
D .
表示向一定量的氢氧化钠溶液中滴加稀硫酸至恰好完全反应
D .  表示将等质量的大理石分别与足量的等质量等溶质质量分数的稀盐酸反应
表示将等质量的大理石分别与足量的等质量等溶质质量分数的稀盐酸反应
|
选项 |
物质 |
目的 |
主要实验操作 |
|
A |
双氧水、蒸馏水 |
鉴别 |
取样,加二氧化锰,观察现象 |
|
B |
CH4中是否含有H2 |
检验 |
点燃,罩一干冷烧杯,观察燃烧产物 |
|
C |
KCl与MnO2固体混合物 |
分离 |
加水充分溶解后过滤、洗涤、烘干,蒸发 |
|
D |
FeSO4溶液(CuSO4) |
除杂 |
加过量Fe粉、过滤 |



写出上图表示的化学方程式为,反应生成的N2与CO2的质量比为。

①已知由氯元素组成的单质是双原子分子,写出图中A点对应物质的化学式。
②与图中的点对应物质类别不相符合的化学式所表示的物质名称是。
③HCl气体是由。(填“分子”、“原子”或“离子”)构成的。






①甲实验的目的是测定空气中氧气的含量
②乙实验,水中的白磷没有燃烧,是因为温度没有达到着火点
③丙实验加水后,立即旋紧瓶盖,振荡,看到的现象是软塑料瓶向内凹陷
④丁实验,酒精灯上放的金属网罩是为了提高温度

|
选项 |
X |
Y |
|
| A | 水 | 氧化钙 | |
| B | 水 | 硝酸铵 | |
| C | 浓硫酸 | 水 | |
| D | 稀硫酸 | 镁 |
A 钢筋混凝土
B 玻璃钢
C 碳纤维复合材料
D 有机玻璃

①图中标识的物质,属于金属材料的是 (写出一种即可)。
②某品牌饮料的空易拉罐应收入 (填 “可回收”或“不可回收”)筒中。
③铁制品锈蚀的过程,实际上是铁跟空气中的 发生化学反应的过程。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3-
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则溶液中一定有Al3+、Fe3+、Cu2+ , 可能有Ag+
A 样品中一定含有镁
B 样品中一定不含有银,可能含有镁
C 所得溶液中溶质总质量为12g
D 加入的稀硫酸的溶质质量分数为19.6%

①用过氧化氢溶液与二氧化锰混合制氧气
②用锌粒与稀硫酸反应制取氢气
③用无水醋酸钠固体与碱石灰固体在加热的情况下制CH4
[提出问题]固体样品的成分是什么?
①碱石灰干燥剂是CaO和NaOH的混合物。
②BaCl2溶液是中性。
[猜想与假设]
固体样品中可能含有Fe、Fe2O3、 CaO、 NaOH、Ca(OH)2、Na2CO3和等七种物质。

甲组同学对滤渣B的成分进行探究,记录如下:
| 实验操作 | 实验现象 | 实验结论及化学方程式 |
| 取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ① ② | 结论:滤渣B中有Fe2O3、CaCO3。实验操作中反应的化学方程式为: |
乙组同学对滤液C的成分进行了探究。记录如下:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有 |
①乙组同学实验中加入过量BaCl2溶液的目的是。
②通过以上实验探究。该固体样品中能确定一定含有的成分是。
