①将10.6g Na2CO3溶于100mL水中
②将28.6g Na2CO3•10H2O溶于少量水中,再用水稀释至100mL
③将20mL 5.0mol/L Na2CO3溶液用水稀释至100mL.
①氢氧化钠溶液 ②硫酸钙固体 ③铜 ④蔗糖 ⑤三氧化硫 ⑥熔融氯化钠.
①花生油加入到水中后充分搅拌;
②向蒸馏水中加入硝酸钾至恰好饱和;
③饱和氯化铁溶液中逐滴加入少量氢氧化钠溶液;
④氢氧化钡溶液中通入过量的CO2;
⑤用滤纸过滤氢氧化铁胶体后得到的滤液;
⑥将纳米材料分散在塑料中制备复合材料;
⑦碘水和酒精的混合物
属于浊液的是:;属于溶液的是:;属于胶体的是:.
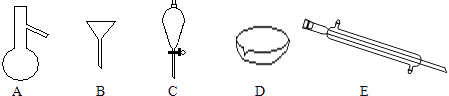
①NaCl固体和泥沙:②花生油和水:
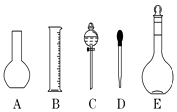
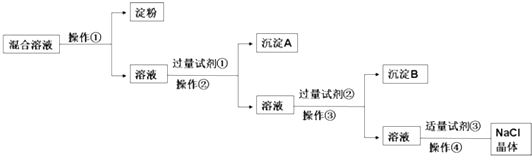
试剂①;试剂③.
编号 | 实验操作 | 预期现象和结论 |
① | ||
② | ||
试通过计算和推理完成下面的问题: