
| 选项 | 实验操作 | 现象 | 结论 |
| A | 往 | 溶液开始无明显变化,最后变成红色 | |
| B | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀,有刺激性气体产生 | 浓硫酸有脱水性和强氧化性 |
| C | | 无明显现象 | |
| D | 将一小块 | 产生气泡 | |
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 锌的金属活动性比铁强 | 在海轮外壳上装锌块可减缓外壳腐蚀 |
| B | 汽油和植物油都属于烃 | 汽油和植物油都可以燃烧 |
| C | 铜绿的主要成分是碱式碳酸铜 | 铜绿在空气中受热分解能得到铜单质 |
| D | | |

| | 0 | 5 | 10 | 20 | … |
| | 0.0 | 8.96 | 15.68 | 22.40 | … |
下列判断正确的是( )
实验流程如下:

乙醚的作用为,操作Ⅰ所需的玻璃仪器除烧杯外还有。
向三颈烧瓶中加入0.10g钨磷酸催化剂和30 30%双氧水,在室温下搅拌5
,然后加入5.0
试剂X,在100℃左右回流反应3h,得到溶液A。
环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X的最佳选择是_______(填序号)。

取0.2g己二酸晶体样品于锥形瓶中,加水溶解,滴加2滴酚酞试液,用
溶液滴定;平行滴定3次,
溶液的平均用量为V
,则己二酸纯度为。(己二酸化学式量为146)
![]()
![]()
| 时间/ | 0 | 10 | 20 | 30 | 40 |
| 总物质的量/ | 1.00 | n1 | n2 | n3 | n4 |
| 总压强/100 | 1.00 | 1.25 | 1.35 | 1.40 | 1.40 |
①n4=,平衡时乙苯的转化率为。
②列式计算t℃下该反应的平衡常数
。(
为以分压表示的平衡常数,计算结果保留1位小数)

①图中A、B、C三点对应平衡常数大小顺序为。
②图中投料比( 、
、
)的大小顺序为,理由是。

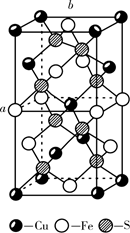
①下列关于气态 和
的说法中,正确的是。
A.中心原子的价层电子对数目相等 B.都是极性分子
C.中心原子的孤对电子数目相等 D.都含有极性键
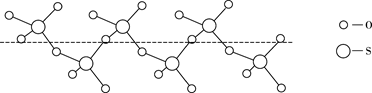
②将纯液态 冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如下图所示,此固态
中S原子的杂化轨道类型是。
③ 、
中S的化合价均为+6.与
互为等电子体的分子的化学式为,
中过氧键的数目为。

已知:核磁共振氢谱表明D只有一种化学环境的氢。
回答下列问题:
 的合成路线
的合成路线