 B . 氯化氢的电子式:
B . 氯化氢的电子式:  D . 硝基苯的结构简式:
D . 硝基苯的结构简式: 
 B .
B .  C .
C .  D .
D . 
 +3H2
+3H2  加成反应
C . nCH2=CH2
加成反应
C . nCH2=CH2 



| 选项 | 实验 | 结论 |
| A | 乙醇和水都能与金属钠反应产生可燃性气体 | 乙醇分子中的羟基氢与水分子中的氢具有相同的活性 |
| B | 向乙酸乙酯中加入足量NaOH溶液,充分振荡,得 到无色透明溶液 | 乙酸乙酯在碱性条件下能发生水解 |
| C | 将混有乙烯的乙烷气体通入酸性高锰酸钾溶液中,溶液颜色变浅 | 乙烯被氧化,可用酸性高锰酸钾溶液除去乙烷中的乙烯 |
| D | 取绿豆大的钠和钾分别投入水中,钾反应更剧烈 | 金属性:K<Na |
 与
与  ④CH4与CH3CH2CH3⑤CH3CH3与
④CH4与CH3CH2CH3⑤CH3CH3与  。
。 其中互为同位素的是(填序号,下同),互为同系物的是。
a.2CO2+6H2 CH3CH2OH+3H2O
b.CO2+CH4 CH3COOH
以上反应中原子利用率较高的是(填字母。)
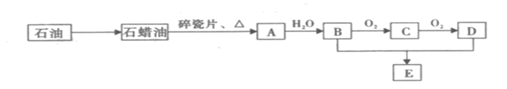
回答下列问题:
①A元素最外层电子数是次外层电子数2的倍;
②B的阴离子和C的阳离子与氖原子的电子层结构相同;
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移;
④C的单质与B的单质在加热条件下反应,生成淡黄色固体,该淡黄色固体能与AB2反应生成B的单质;
⑤D的气态氢化物的化学式为H2D。回答下列问题:
a.D的简单气态氢化物比E的稳定
b.高温灼烧C、E形成的化合物,火焰呈紫色
c.物质AB2的结构式为O=C=O

①2~6min内用稀盐酸表示的平均反应速率为(精确到0.0001)mol•L1•min-1。
②从图可以看出,4min后反应速率逐渐减慢,原因是。

①若电解质溶液为稀硫酸,则Mg上发生的电极反应式为,当有2.4gMg溶解时,Al电极上生成(标准状况)L氢气。
②若电解质溶液为NaOH溶液,则外电路中的电子(填“流出”或“流入”)Al电极。

①装置A中苯发生反应的化学方程式为。
②反应进行一段时间后,装置C中的现象是。
③装置B是吸收瓶,如果没有装置B而将A、C直接相连,你认为是否妥当?(填“是”或“否”),原因是。
④实验完毕后,将装置A中的液体倒入装有冷水的烧杯中,烧杯(填“上”或“下”)层为溴苯。