 B . 量取9.5mL液体
B . 量取9.5mL液体  C . 测定未知溶液的pH
C . 测定未知溶液的pH 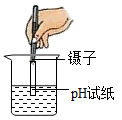 D . 稀释浓硫酸
D . 稀释浓硫酸 

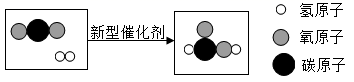
选项 | 事实 | 解释 |
A | Fe、Fe2+、Fe3+化学性质不同 | 微粒中的质子数不同 |
B | 水通电产生氢气和氧气 | 在化学变化中分子可分,原子不可分 |
C | 稀盐酸、稀硫酸均显酸性 | 溶液中都含有氢元素 |
D | 冰水混合物属于纯净物 | 冰和水都含有相同原子 |




|
资料: 1.氦气是有刺激性气味的无色气体,密度比空气小,极易溶于水,其水溶液显碱性。 2.加热熟石灰和氯化铵的固体混合物生成氨气。 |
Ⅰ.制取氨气还缺少的仪器名称是,装药品前要。
Ⅱ.若用图2装置收集氨气,进气口应为端(选填“m”或“n”)。

(查阅资料):①氢氧化钙微溶于水(20℃时,100克水中最多溶解0.165克氢氧化钙)②氢氧化钙水溶液可以使无色酚酞溶液变红色。

探究二:生石灰变质后的成分是什么?
|
实验操作 |
现象 |
结论和解释 |
|
取生石灰样品少许放入烧杯中加水搅拌插入温度计(如图2) |
形成浊液,温度(升高、降低或不变) |
结论:生石灰已变质,解释:。 |
|
实验操作 |
现象 |
结论和解释 |
|
取生石灰样品少许放入烧杯中加水搅拌,过滤,向滤液中滴加酚酞溶液,向滤渣滴加足量的(填试剂名称)。 |
滤液变色;滤渣上产生大量气泡。 |
结论:猜想③符合题意。解释:生石灰变质过程中产生碳酸钙的化学方程式是 |
方案一:取10.0g样品加100克水搅拌溶解过滤将固体干燥后称量为9.8g,计算得到碳酸钙的质量分数为98.0%.方案一是否合理?理由是。
方案二:取10.0g样品,请设计完成方案二,同时说明要测定的量(用a表示),并计算样品中碳酸钙的质量分数。(不要求写出计算过程)。
