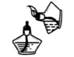
 C . 加热高锰酸钾
C . 加热高锰酸钾  D . 收集氧气
D . 收集氧气 


①某种物体的放大或缩小的复制品
②可以是一幅图、一张表或计算机图像
③可以表示一个过程,如描述水的三态变化的示意图
④有的模型是抽象的,如一些数学公式
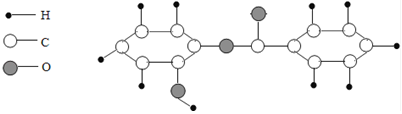
①该物质的一个分子由二十六个原子构成 ②该物质是氧化物
③该物质中碳、氧元素的质量比是156:48 ④该物质的相对分子质量是214g
⑤该物质是有机高分子化合物 ⑥该物质由碳、氢、氧三个元素组成
⑦该物质的化学式为C13H10O3


| 消毒剂类型 | 成分 | 使用注意事项 |
| 含氯消毒剂 | 84消毒液(有效成分NaClO) | 不能与洁厕灵(含盐酸)混用 |
| 醇类消毒剂 | 医用酒精(C2H5OH含量为75%) | 远离火源 |
| 过氧化物类消毒剂 | 过氧化氢(H2O2)消毒剂 | 见光或受热易分解,有腐蚀性、有灼伤危险 |
| 过氧乙酸(CH3COOOH)消毒剂 |
下列有关上述常用消毒剂的分析,错误的是( )

| 物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
下列判断正确的是 ( )

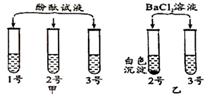
甲实验:根据现象,可鉴别出1号试管中的溶液;
乙实验:观察到2号试管中有白色沉淀。

①将导管伸入集气瓶口,气体进入瓶中
②将装满水的集气瓶倒置在水槽中的塑料支架上(D图中支架略去)
③当集气瓶中的水被全部排出后,用毛玻璃片盖上瓶口,将集气瓶移出水面放置备用.
④导管口出现均匀的气泡




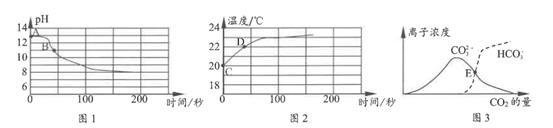
查阅资料:本实验条件下,Na2CO3 溶液与NaHCO3溶液的pH分别约为11.0 和8.5
|
烧杯编号 |
A |
B |
C |
|
加水的质量/克 |
80 |
100 |
120 |
|
溶液的质量/克 |
113 |
140 |
160 |

①通过计算说明,该食用纯碱中碳酸钠的质量分数是否与包装袋信息相符。(计算结果精确到0.1%)
②有同学认为小明测定的食用纯碱中碳酸钠的质量分数会偏大,请分析造成碳酸钠质量分数偏大的主要原因是 ▲ 。
|
加入稀盐酸质量/g |
25 |
50 |
75 |
100 |
|
产生的气体质量/g |
1.1 |
2.2 |
3.3 |
3.52 |

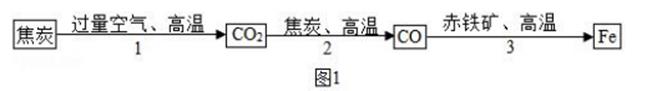
①自热火锅食用方法:下层底盒中倒入适量冷水,打开加热包塑料膜,将加热包放入凉水中:放上上层食材盒,倒入一定食用冷水,盖上盖子,15分钟后,即可开盖食用。(图乙为自热火锅结构示意图)
②加热包内含有铁粉、铝粉、焦炭粉、生石灰等物质,其中的金属粉末与碳粉在热水中发生化学反应,可短时间放出大量的热,后续缓慢放热。
③自热火锅工作时,下层加热盒中空气温度随时间变化的图像如下图丙所示。
为解释自热火锅的工作原理,请结合上述材料,对oa、ab、bc各段的温度变化做出解释:。

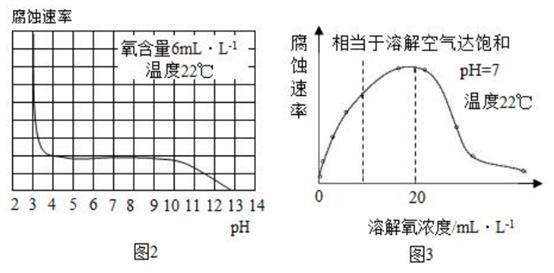
①图2表示水样温度22℃、氧含量6mL/L时,钢铁腐蚀速率与水样pH的关系。当pH<4时,随pH值减小,钢铁腐蚀速率明显增大的原因是。
②图3表示温度22℃、pH=7时,钢铁腐蚀速率与水中溶解氧浓度的关系。当溶解氧超20mL/L时,钢铁腐蚀速率明显下降的原因可能是。
Ⅰ.“暖宝宝”贴片内含有铁、活性炭、无机盐、水等物质,可在空气中吸收氧气发生放热反应,反应过程中主要的化学方程式为:2Fe+O2+H2O=2Fe(OH)2;"暖宝宝"贴片吸氧能力强,放热迅速。
Ⅱ.空气中氧的体积约占空气体积的1/5;封闭气体的压强与气体温度、气体体积和气体质量有关,气体的温度升高、体积变小、质量变大都会引起气体压强的增大。
|
思维模型 |
①构建封闭体系 |
②改变气压 |
③观察现象 |
④得出结论 |
|
检验过程 |
将瓶子放入水中,盖好瓶塞 |
将瓶子向下压或用手捧住容器 |
观察到 |
说明装置气密性良好 |

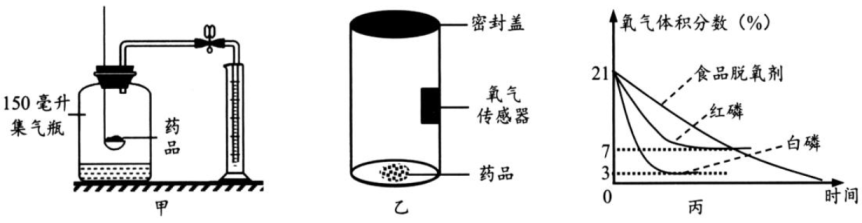
①准备如图乙的玻璃容器,顶部用密封盖密封,并检查该装置的气密性。
②将氧气传感器(能实时显示容器内氧气的体积分数)固定在容器内壁,并装入足量的红磷。
③用激光笔点燃红磷,红磷剧烈燃烧,观察并记录氧气传感器所显示的氧气体积分数的变化情况。
④用白磷替换红磷重复上步骤①~③。
⑤换用食品脱氧剂(可以直接与氧气反应,无需点燃的物质)重复上述步骤①~③。
根据实验数据,分别绘制三种物质氧化时容器内氧气体积分数随时间的变化情况,如图丙所示。
猜想一:O2中的O元素全部来源于CO2;
猜想二:O2中的O元素全部来自于H2O;
猜想三:O2中的O元素来源于CO2和H2O。
为了求证,他们查阅了以下资料:
资料一:范尼尔通过实验得出紫硫细菌合成有机物的反应式,与高等植物光合作用的
反应式进行比较研究后,建立了猜想。
紫硫细菌:CO2+2H2S (CH2O)(糖类)+2S+H2O
高等植物:CO2+2H2O (CH2O)(糖类)+O2+H2O
资料二:美国科学家鲁宾、卡门给三组小球藻提供含有一定比例180的水和碳酸氢盐(碳酸氢盐给小球藻的光合作用提供全部的CO2 , 而且不产生水,其他条件均相同),光照相同时间后,分别检测小球藻释放氧气中18O的比例,实验结果如表所示。(18O可作为示踪原子)
|
组别 |
水中18O的比例(%) |
碳酸氢盐中18O的比例(%) |
释放的氧气中18O的比例(%)| |
|
1 |
0.85 |
0.41 |
0.84 |
|
2 |
0.85 |
0.55 |
0.85 |
|
3 |
0.85 |
0.61 |
0.85 |
资料三:
Ⅰ.16O表示中子数为 8的氧原子,18O是表示中子数为10的氧原子, 所以1个18O的质量是一个16O的质量9/8倍;自然界的氧气在标准状况下的密度为1.43千克/米3 , 其中16O占99.76% (可视为100%) ;
Ⅱ.在相同的温度和压强下,相同体积的气体具有相同的分子数。
Ⅲ.鲁宾和卡门通过测生成氧气的密度来确定氧气中18O含量。

步骤一:向大烧杯中注入足量的冷水,打开K1关闭K2 , 向下压左侧注射器活塞,使生成的氧气持续通入U形管,并观察U形管中现象;
步骤二:关闭K1、打开K2 , 向下压右侧注射器活塞,使生成的二氧化碳将U形管内的氧气排尽,然后将烧杯中的冷水换成等量的80℃的热水,并观察U形管中现象;
步骤三……并观察U形管中现象。